Nanopartikel an der Blut-Hirn Schranke
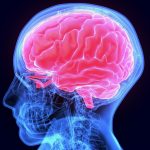
Die Blut-Hirn-Schranke ist die Trennung zwischen dem Blutgefäßsystem und dem Gehirn und wird von bestimmten Zellen (sogenannte Endothelzellen) gebildet, welche die Blutgefäße im Gehirn umschließen. Diese Barriere ist für Nanopartikel normalerweise undurchlässig. Die Blut-Hirn-Schranke trennt das Blutgefäßsystem und das Gehirn voneinander ab [1]. Unsere Blutgefäße sind mit bestimmten Zellen (Endothelzellen) ausgekleidet, die besonders im Gehirn […]
WeiterlesenNanopartikel und die Riechschleimhaut
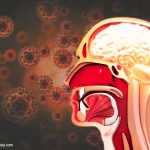
Die Riechschleimhaut ist ein Gewebe, das sich bei Säugetieren also auch beim Menschen in der Nase befindet, besser gesagt dem oberen Teil der Nasenmuschel, dem Nasendach. Hier strömt die eingeatmete Luft an freien Nervenendigungen vorbei. Alles was dort in die Nervenzellen hineingelangt, kann unter Umständen auch direkt zum Riechkolben und von dort direkt ins Vorderhirn […]
WeiterlesenNanopartikel und die Lunge
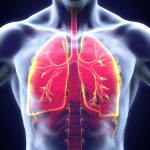
Der Begriff Blut-Luft-Schranke beschreibt eine dünne zelluläre Trennschicht innerhalb der Lunge, die den luftgefüllten Raum der Lungenbläschen vom Blutkreislauf abgrenzt. Über diese Schranke wird die Aufnahme von Sauerstoff in das Blut und die Abgabe von Kohlenstoffdioxid in den Lungenraum geregelt. Mit der Atemluft können auch körperfremde Objekte abhängig von ihrer Größe in die Lunge gelangen. […]
WeiterlesenNanopartikel und die Haut
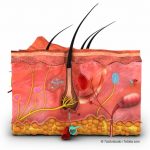
Die Haut ist das größte Organ des Körpers. Durch Abgrenzung von Innen und Außen schützt sie den Körper gegen die unterschiedlichsten Einwirkungen z.B. vor mechanischen Einflüssen wie Druck, Stoß, Zug, Reibung oder Verletzungen. Nanopartikel können die intakte Haut nicht durchdringen. Auch leichte oberflächliche Verletzungen beeinträchtigen diesen Schutz nicht. Kleinere mechanische Beanspruchungen der Haut fängt die […]
WeiterlesenNanopartikel und das Immunsystem

Das Immunsystem erkennt sowohl fremde als auch körpereigene Stoffe. Werden Fremdstoffe wie z.B. Nanopartikel erkannt, so entscheiden Zellen des Immunsystems, ob eine Gefahr vorliegt oder nicht. Schätzt der Körper den erkannten Fremdstoff als gefährlich ein, reagiert er darauf mit einer Entzündung. Im Falle von Krankheitserregern werden diese zunächst vom Abwehrprogramm eingegrenzt, dann beseitigt und falls […]
WeiterlesenNanopartikel und der Magen-Darm-Trakt
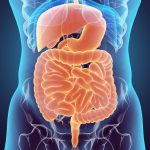
Unser Magen-Darm-Trakt ist hochspezialisiert, wenn es darum geht, Material (Nahrung) von außen aufzunehmen und diese in gebrauchsfertigen, zerkleinerten Einheiten über das Blut auf die Organe zu verteilen. Es besteht die Möglichkeit, dass auch Nanomaterialien diese Körperschranke durchdringen können. Es handelt sich jedoch um nur sehr kleine Mengen, deren Wirkung bisher als unbedenklich eingestuft wird. Nahrung […]
WeiterlesenWie entsorgt der Körper Nanopartikel?
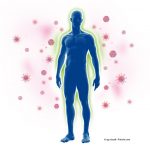
Im Körper vorhandene Nanopartikel (z. B. durch Injektion) werden in der Mehrzahl durch das sog. Retikulohistiozytäre System (RHS) aufgenommen und entsorgt. Dieses System stellt ein Netzwerk von Zellen dar. Die Zellen des RHS haben die Aufgabe, tote Zellen, Bakterien, Viren und eingedrungene Kleinpartikel zu inaktivieren und zu eliminieren. Zu diesen partikulären „Eindringlingen“ gehören auch Nanopartikel. […]
WeiterlesenNanopartikel an der Plazentaschranke
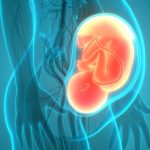
Die Plazenta ist eine wichtige Gewebeschranke, die das ungeborene Kind von der Mutter trennt. Dieses ist dabei vollständig abhängig vom richtigen Funktionieren der Plazenta, da sie für die Versorgung mit Sauerstoff und Nahrung zuständig ist, aber auch Kohlenstoffdioxid und Abfallstoffe abtransportiert. In diesen Prozessen können auch Nanopartikel transportiert werden und den Fötus erreichen. Die […]
Weiterlesen >
>