Titandioxid Nanopartikel sind unter anderem in Sonnencremes und speziellen Wandfarben enthalten. Man kann damit also vor allem über die Haut in Kontakt kommen. Titandioxid ist nicht mehr als Lebensmittelzusatzstoff zugelassen . Eine außergewöhnliche Gefährdung speziell durch die Nanoform ist nicht erkennbar.

Kind mit Sonnencreme © Sunny-studio/fotolia.com
Wie könnte ich damit in Kontakt kommen?
In Sonnencreme trägt man Titandioxid Nanopartikel auf die Haut auf. Gesunde und sonnenverbrannte Haut wird dabei nicht durchdrungen. Wunden sollte man stattdessen mit Wundsalbe versorgen. Als Wandfarbe werden Titandioxid Nanopartikel für selbstreinigende Fassaden eingesetzt. Sobald die Farbe getrocknet ist, ist das Titandioxid fest mit dem Anstrich verbunden; Menschen werden auf diesem Weg nicht belastet. In Kacheln, Pflastersteinen, Solarzellen etc. ist Titandioxid ebenfalls fest gebunden; Nanopartikel werden im täglichen Gebrauch nicht frei, so dass sie auch nicht in den Körper gelangen. In allen Fällen können die Nanopartikel aber aus dem festen Verbund heraus gewaschen werden, so dass sie in die Umwelt gelangen. Bislang konnte dadurch keine schädliche Wirkung festgestellt werden; das muss aber weiter untersucht werden.
Wie gefährlich ist das Material für Mensch und Umwelt?
Titandioxid wirkt in sehr großen Mengen giftig. Grundsätzlich sollte man das Einatmen aller Stäube vermeiden. Im Tierversuch wurden Schädigungen nach hoher Dosierung in der Lunge nachgewiesen. Diese und weitere Studien haben auch dazu geführt, dass Titandioxid ab August 2022 in der EU nicht mehr als Lebensmittelfarbe E 171 zugelassen ist, für Medikamente gilt dieses Verbot nicht.
Fazit
Titandioxid Nanopartikel können nicht durch unverletzte Haut in den menschlichen Körper gelangen. In anderen Anwendungen sind Titandioxid Nanopartikel fest an andere Materialien gebunden und liegen somit nicht als freie Partikel vor.
Nebenbei
- Bei Schleif- oder anderen Renovierungsarbeiten wird immer Staub frei, der Nanoanteile enthält – unabhängig davon, ob vorher Nanopartikel in dem bearbeiteten Material enthalten waren. Nassschleifen reduziert den Staubanteil in der Luft und verhindert auch die Bildung von Nanoteilchen
Eigenschaften und Anwendungen
Titandioxid (chemisch TiO2) ist mittlerweile zu einem alltäglichen Begleiter in unserem Leben geworden. Man findet es in Konsumgütern wie bspw. Kosmetika, in Farben und Lacken, in Textilien, Papier und Kunststoffen, in Medikamenten oder mittlerweile sogar in Pflastersteinen: Viele Alltagsprodukte nutzen Titandioxid. 2009 wurden weltweit 4,68 Millionen Tonnen Titandioxid produziert, innerhalb der EU sind es 1,5 Mio. Tonnen pro Jahr.
Dies hat es vor allem seiner Vielseitigkeit in Größe und Gestalt zu verdanken. Mal kommt es als mikroskaliges Pigment zum Einsatz, mal als Nanoobjekt. Auch seine Kristallstruktur kann variieren; je nach Anordnung der Atome unterscheidet man die Rutil-und die Anatas-Modifikation.
Am häufigsten wird Titandioxid als Weißpigment eingesetzt, da es einen hohen Brechungsindex hat und somit in der Lage ist, das einfallende Licht stark zu streuen und zu reflektieren. Deshalb und wegen seiner hohen UV-Beständigkeit gilt es als das Standardpigment für weiße Dispersionsfarben mit hoher Deckkraft. Die Weißpigmente aus Titandioxid sind fast ausschließlich Partikel in der Rutilmodifikation mit Korngrößen im Mikrometerbereich, da der Effekt der Lichtstreuung bei zu kleinen - nanoskaligen - Partikeln nicht mehr auftritt. Dieses weiße Pigment findet nicht nur in Farben, sondern auch in Lacken, Kunststoffen, Papier sowie Textilien Verwendung. Unter der Kennzeichnung E171 wurde es bis zum Verbot im August 2022 in der EU als Lebensmittelzusatzstoff geführt, es ist aber in Zahncremes, verschiedenen anderen Kosmetika und Medikamenten nach wie vor erlaubt. Am schnellsten wächst derzeit der Markt für Titandioxid-Pigmente für den Einsatz in Kunststoffen. Insbesondere die hohe Nachfrage der Verpackungsindustrie führt hier zu steigendem Verbrauch an Titandioxidpigmenten.

Flasche Sonnencreme im Sand © vimarovi/ Fotolia.com
Nanoskaliges Titandioxid, das für spezifische Anwendungen hergestellt wird, ist etwa um den Faktor 100 feinteiliger als die Pigmentform und weist andere physikalische Eigenschaften auf. Das Produktionsvolumen von nano-Titandioxid beträgt weniger als 1 % der produzierten Menge von Titandioxid-Pigmenten. Derzeit wird es vor allem als Wirkstoff in Sonnencremes, Textilfasern oder Holzschutzmitteln genutzt. Der Industrieverband Körperpflege und Waschmittel e.V. berichtet, dass Titandioxid derzeit in Sonnenschutzmitteln ausschließlich in seiner Nanogestalt vorkommt. Zudem ist es mit weiteren Materialien beschichtet, um bessere Dispersionseigenschaften zu erhalten und die Photostabilität zu gewährleisten. Verglichen mit den lange in Sonnencremes eingesetzten Titanoxid-Mikropartikeln, die klebrige und alles andere als einfach und angenehm auf die Haut aufzubringende Pasten ergaben und zudem einen deutlichen weißen Film auf der Haut hinterließen, ist nanoskaliges Titandioxid dagegen transparent und lässt sich wesentlich leichter auftragen. Die Schutzwirkung gegen UV-Strahlung ist zudem bei Nanopartikeln wesentlich besser.

Eine weitere Eigenschaft von Titandioxid ist seine photokatalytische Aktivität, die durch das hohe Oberflächen/Volumen-Verhältnis von Nanopartikeln im Vergleich zu Mikropartikeln gesteigert wird. Jedoch ist nicht jede Modifikation hierfür geeignet. Anders als in den bislang genannten Anwendungen in Lichtschutz und Farben, bei denen vor allem Rutil-Titandioxid zum Einsatz kommt, ist für die Photokatalyse vor allem die Anatas-Modifikation geeignet. In Gegenwart von UV-Strahlung kann Anatas-Titandioxid aus Wasser bzw. Luft Radikale bilden, die organische Schadstoffe oxidativ abbauen können. In Japan sind entlang von Verkehrswegen Pflastersteine und Kacheln im Einsatz, die mit Hilfe von Titandioxid die Luft von Autoabgasen „befreien können“. Forscher an der Universität Kassel fanden einen Weg nano-Titandioxid mit Farbstoffmolekülen derartig zu verzahnen, dass der photokatalytische Prozess auch durch sichtbares Licht und nicht ausschließlich durch UV-Strahlung ausgelöst werden kann.
Aufgrund des hydrophilen Charakters von Titandioxid bildet Wasser auf derartigen Oberflächen einen geschlossenen Film, welcher Schmutz und Abbauprodukte leicht abtransportieren kann. Titandioxid-Partikel, eingebracht in Fassadenfarben oder Kacheln, führen somit zu selbstreinigenden, schmutzabbauenden Oberflächen. Die hydrophilen Eigenschaften des nanoskaligen Titandioxids werden zudem bei sog. „Anti-Fog“-Beschichtungen ausgenutzt. Der ultradünne Wasserfilm auf einer Glasscheibe, die mit einer transparenten Schicht von nanoskaligem Titandioxid beschichtet wurde, verhindert die Bildung von Wassertröpfchen und folglich auch das Beschlagen. Ein weiteres Anwendungsgebiet von nanoskaligem Titandioxid sind Farbstoffsolarzellen (Grätzel-Zellen).
Titandioxid ist als nanometergroßes Pulver nicht selbstentzündlich. Auch als fein verteilte Mischung mit Luft (Staub) unter Einwirkung einer Zündquelle ist es nicht entzündlich. Es besteht keine Möglichkeit einer Staubexplosion.
Natürliches Vorkommen und Herstellung
Titandioxid kommt meist in Verbindung mit anderen Gesteinsarten vor und muss von diesen abgetrennt werden. Eines der bekanntesten Mineralien ist das Ilmenit (FeTiO3). Zur Raffinierung dieser Vorkommen werden unterschiedliche Verfahren genutzt.
In der EU wird Titandioxid zu 70 Prozent nach dem Sulfatverfahren aus natürlichen Mineralien gewonnen, während die verbleibenden 30 Prozent nach dem Chloridverfahren gewonnen werden. In Deutschland sind beide Verfahren zu gleichen Teilen vertreten. Das Sulfatverfahren geriet vor einigen Jahrzehnten in die Kritik, da hier verdünnte Schwefelsäure (sog. Dünnsäure) entsteht, die bis in die 1980er Jahre in der Nordsee verklappt wurde. Seit 1990 ist dies in Deutschland verboten. Die Dünnsäure wird nun aufbereitet oder in andere Herstellungsprozesse eingeleitet. Beim Cloridverfahren reagieren die Titandioxid-Erze mit Chlorgas unter Bildung von Salzsäure. Diese kann zum einen wieder in den Produktionsprozess zurückgeführt werden und ist zudem industriell weitaus bedeutender und kann somit auch verkauft werden.
Zur Produktion von nanoskaligem Titandioxid sind weitere Prozesse notwendig. Zum Einen können sogenannte Titan-Alkoxylate hydrolisiert und anschließend thermisch behandelt werden. Hierbei ist es abhängig von der Temperatur welche Kristallmodifikation die Partikel nach dem Prozess haben. Des Weiteren werden nanoskalige Titandioxid-Partikel durch die Umsetzung von Titanchlorverbindungen mit Ammoniak hergestellt. Das entstehenden Titanoxidhydrat geht unter Wärmeeinwirkung in Rutil-Titandioxid über. Ein in den 1940er Jahren von der Degussa entwickeltes Verfahren, das sog. Aerosilverfahren, wurde in den 1950er Jahren von Siliziumdioxid auf Titandioxid übertragen. Dadurch ist es ebenfalls möglich aus Titanchlorverbindungen mittels Umsetzung mit Wasserdampf zu nanoskaligem Titandioxid zu gelangen.
NanoCare - Datenblätter
- Titandioxid Datenblatt Nr.1 (PDF)
- Titandioxid Datenblatt Nr.2 (PDF)
- Titandioxid Datenblatt Nr.3 (PDF)
- Titandioxid Datenblatt Nr.4 (PDF)
- Titandioxid Datenblatt Nr.5 (PDF)
Weiterführende Informationen
- PR Web.com (EN) (30.08.2010) . Global Titanium Dioxide Industry Stabilises and Heads for Recovery, TZMI Pressemitteilung.
- Cefig.org (EN): Titanium Dioxide Manufacturers Association (TDMA) (Stand letzter Zugang: Sep 2011).
- Cefig.org (EN): Industry responds to Nano-TiO2 study published in American Association for Cancer Research Journal, Offener Brief des Titanium Dioxide Stewardship Council vom 3. März 2010.
- Schweizer Kosmetik- und Waschmittelverband (SKW) (02.09.2014). Nanomaterialien in Kosmetika. (PDF; 38 KB)
- NanoTrust Dossier No.008 (Jan 2009). Nanotechnologie in Kosmetika, NanoTrust, Institut für Technikfolgen-Abschätzung (ITA), Wien.
- Scientific Committee on Consumer Products (SCCP) (19.06.2007). Safety of nanomaterials in cosmetic products.
Titandioxid wird in vielen Produkten des täglichen Lebens eingesetzt. Eine Neubewertung einiger vorhandener Studien führte im Jahr 2020 zu Bedenken. Wenn Titandioxid in großen Mengen eingeatmet wird, kann dies ein gewisses Lungenkrebsrisiko darstellen. Aus diesem Grund wurde die Verwendung stark eingeschränkt. In Lebensmitteln wurde Titandioxid 2022 verboten.
Kontakt im Alltag
Obwohl epidemiologische Studien bisher keine Hinweise auf eine erhöhte Gefährdung von Arbeitnehmern oder Verbrauchern liefern, wurde die Verwendung von Titandioxid in Lebensmitteln als Zusatzstoff in der EU 2022 verboten. In Produkten des täglichen Gebrauchs muss es gesondert ausgewiesen werden. Die Neueinstufung im Jahr 2021 beruht auf Versuchen mit Ratten und sehr hohen verabreichten Dosen. Im Alltagsprodukten sind jedoch die in den Studien eingesetzten Mengen an Titandioxid nicht zu erwarten.
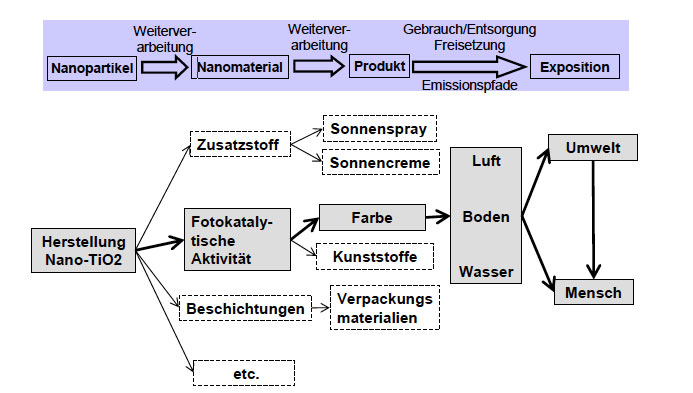
Lebenszyklus und mögliche Freisetzungspfade von Titandioxid. © Kuhlbusch et al., 2010, UBA-Studie.
Situation am Arbeitsplatz
Bisher liefert keine der epidemiologischen Studien Hinweise auf eine erhöhte Gefährdung für die Mitarbeiter in der Produktion an Lungenkrebs oder anderen Krebsarten zu erkranken. Auch die Sterblichkeitsrate ist nicht erhöht .
Arbeitsplatzexpositions-Studien im Rahmen des Projektes NanoCare zeigten, dass beim Abfüllen von Titandioxid-Pulver hauptsächlich Partikel freigesetzt werden, die größer als 450 nm sind. Es handelt sich hierbei also nicht um Nanopartikel .
Dennoch ist das Risiko Titandioxid-haltige Stäube einzuatmen am Arbeitsplatz in der verarbeitenden Industrie am höchsten. Aus diesem Grund gelten selbstverständlich alle relevanten Grenzwerte der sogenannten „granulären biobeständigen Staubpartikel“ (GBS, siehe auch Granuläre biobeständige Stäube) auch für Titandioxid-Partikel unabhängig von ihrer Größe.
Situation beim Verbraucher
Verbraucher konnten bisher über alle Aufnahmewege mit Titandioxid in Kontakt kommen. Als UV-Filter in Sonnenschutzmitteln oder Kosmetika oder als Farbpigment in Wandfarben über die Haut, als Lebensmittelzusatzstoff über die Nahrung oder bei Schleifarbeiten auch über die Lunge.
Da seit 2022 Titandioxid in Nahrungsmitteln verboten ist und es auch in Kosmetika seitens der Hersteller nur noch eingeschränkt eingesetzt wird, sind diese Aufnahmewege erheblich reduziert, obwohl es bisher keine Indizien für negative Effekte durch Titandioxid in diesen Produkten gibt. Titandioxid ist in Medikamenten als Hilfsstoff weiterhin zugelassen, da es keinen Ersatz dafür gibt. Ein Verbot in Medikamenten würde eine weitere Verknappung von wichtigen Medikamenten auf dem Europäischen Markt bedeuten (seit 2022).
Die Exposition hat nach dem Verbot in Lebensmitteln und den Einschränkungen in Kosmetika erheblich zurückgegangen. Jedoch gab es seit mehr als 40 Jahren keinerlei Hinweise auf irgendwelche gesundheitlichen Effekte bei Verbrauchern für den Einsatz von Titandioxid. Auch am Arbeitsplatz gab es bisher keine Bedenken durch epidemiologische Studien, da diese alle negativ sind.
Further Informationen
- Kuhlbusch, T. (Okt 2010). Emissionen von Nanopartikeln aus ausgewählten Produkten in ihrem Lebenszyklus. UBA-Studie, Umweltbundesamt, ISSN 1862-4804.
- EC (2022): EMPFEHLUNG DER KOMMISSION vom 10. Juni 2022 zur Definition von Nanomaterialien. Download: https://eur-lex.europa.eu/legal-content/DE/TXT/PDF/?uri=CELEX:32022H0614(01)&from=DE
Aufgrund der Anwendung von Titandioxid-Nanopartikeln in Alltagsprodukten wird eine verstärkte Exposition in Gewässern (also der aquatischen Umwelt) erwartet. Dabei ist beispielsweise ein Auswaschen von Partikeln aus Anstrichen/Farben denkbar, die im Außenbereich von Gebäuden verwendet werden und Wind und Regen ausgesetzt sind. Ebenso können Partikel von mit Sonnencreme behandelter Haut während des Badens oder Duschens in Oberflächen- oder Abwasser gelangen.
Der Nachweis von Titandioxid (TiO2) Nanopartikeln in der Umwelt gelang bisher jedoch selten. So wurde die Auswaschung von Titanidioxid-Nanopartikeln aus Fassaden, welche mit TiO2-haltigen Farben gestrichen worden waren, nachgewiesen [1]. Die Partikel gelangten durch herunter laufendes Regenwasser in Form von Aggregaten und oft eingebettet in Farbbestandteile in Oberflächen-Gewässer.
Bei der Untersuchung von Sedimentproben eines Gebietes in China gelang es, technisch hergestellte TiO2-Partikel mittels Elektronenmikroskopie nachzuweisen und diese von natürlich vorkommendem Titan abzugrenzen [2]. Gleichzeitig zeigte diese Studie, dass die Anreicherung der Sedimente mit Titan schon vor Dekaden begonnen hat, da sich auch die früher produzierten gröberen Partikel nachweisen lassen. Als Quellen der Titan-Verschmutzung wird die Einleitung von geklärtem und ungeklärtem Abwasser angenommen.
Eine Untersuchung von Abwässern aus Kläranlagen [3] ergab, dass ein Großteil aller Titanpartikel aus dem Abwasser entfernt wird, jedoch gerade die sehr kleinen (<700nm) Teilchen im Wasser verbleiben und so wieder in Flüsse und Seen gelangen können. Die Titan-Konzentrationen im Ausstrom der Kläranlage betrugen zwischen 5 und 15µg/l. Die meisten Titanpartikel werden während des Klärprozesses an Feststoffe gebunden und gelangen in den Klärschlamm. Dieser wiederum wird entweder auf der Mülldeponie entsorgt oder auf Felder zur Düngung ausgebracht, so dass die gröberen Titanpartikel eher in den Boden gelangen können.
Weil die TiO2-Konzentrationen in der Umwelt so gering sind, stellen sowohl die Entwicklung von Meßmethoden [4,5] als auch die Simulation der Exposition von Titandioxid-Nanopartikel in der Umwelt [6] gegenwärtig Schwerpunkte in Forschung und Entwicklung dar.
Mittels Computerprogrammen wurde versucht zu simulieren, wie sich Titandioxid-Nanopartikel in der Umwelt verhalten könnten. Am wahrscheinlichsten werden sie demnach in natürlichen Oberflächengewässern bzw. in ihren Sedimenten und im Klärschlamm bzw. Böden auf welche Klärschlamm ausgebracht wurde, auftreten [7,8]. Vergleicht man diese berechneten Umwelt-Konzentrationen (PEC Wert) mit für Umweltorganismen gerade nicht gefährlichen Konzentrationen (PNEC Wert), so zeigt sich, dass gegenwärtig von TiO2-Nanopartikeln Risiken für die Umwelt besonders am Ausfluss von Kläranlagen möglich sind. Für Oberflächengewässer, Böden und für die Luft ist nach derzeitigem Kenntnisstand hingegen kein Risiko zu erwarten. Wie ein solches Risiko berechnet wird, ist in der Abbildung genauer erläutert.
Risikoquotienten für TiO2 in verschiedenen Regionen |
|||
| Umweltkompartiment | Europa | USA | Schweiz |
| Oberflächengewässer | 0,015 | 0,002 | 0,02 |
| Kläranlagenausfluss | 3,5 | 1,8 | 4,3 |
| Luft | <0,0005 | <0,0005 | <0,0005 |
Der Risikoquotient wird aus vorhergesagten Umweltkonzentrationen (PEC) geteilt durch die vorhergesagten Konzentrationen, die keine Effekte auf Umweltorganismen haben (PNEC), gebildet. Ist der Risikoquotient kleiner als 1, so besteht gegenwärtig kein Risiko für die Umwelt, bei Werten über 1 besteht ein Risiko und weitere Untersuchungen müssen durchgeführt werden[7].
Eine weitere Computersimulation geht davon aus, dass zukünftig die Menge an produziertem TiO2 weiter steigen wird und dass sich der Anteil an nanoskaligem TiO2 ebenfalls weiter erhöht [9]. Daraus wird abgeleitet, dass sich die Umweltkonzentrationen zukünftig erhöhen werden.
Generell gibt es in diesem Bereich noch große Wissenslücken, welche vor allem unzureichenden Meßmethoden und damit genauen Kenntnissen der Umweltkonzentrationen geschuldet sind. Es fehlen weitere Daten zu genauen Substanzmengen ebenso wie zum Verhalten und zur Verteilung in den 3 Umweltkompartimenten Wasser, Boden und Luft.
Literatur
- Kaegi, R et al. (2008), Environ Pollut, 156(2): 233-239.
- Luo, Z et al. (2011), J Environ Monit, 13(4): 1046-1052.
- Kiser, MA et al. (2009), Environ Sci Technol, 43(17): 6757-6763.
- Tiede, K et al. (2009), Water Res, 43(13): 3335-3343.
- Contado, C et al. (2008), Anal Chem, 80(19): 7594-7608.
- Gottschalk, F et al. (2010), Environ Modell Softw, 25(3): 320-332.
- Gottschalk, F et al. (2009), Environ Sci Technol, 43(24): 9216-9222.
- Mueller, NC et al. (2008), Environ Sci Technol, 42(12): 4447-4453.
- Robichaud, CO et al. (2009), Environ Sci Technol, 43(12): 4227-4233.
Titandioxid kann über die Lunge oder den Magen-Darmtrakt aufgenommen werden. Die Haut ist durch ihre vielen Schichten eine gute Barriere für Partikel. Die Zugabe von Titandioxid in Nanoform zu Lebensmitteln oder Lebensmittel-Verpackungen war in Deutschland nie zugelassen. Seit August 2022 ist Titandioxid (E171) in jeder Form und Größe als Lebensmittelzusatzstoff verboten.
Aufnahme über die Lunge
Im Rahmen des Projekts NanoCare wurden in vitro Test mit humanen Lungenzellen durchgeführt. Verschiedene Varianten von Titandioxid verursachten nur nach Gabe sehr hoher Dosen (≥ 50 µg/cm2) Vitalitätsverluste. Zellen, die zur Simulation der Staubentwicklung für 2 und 4 Stunden im sog. "Karlsruher Expositionssystem" . Titandioxidpartikeln ausgesetzt wurden, zeigten in allen verwendeten Konzentrationen keinen Vitalitätsverlust und es gab keine Anzeichen akuter Zytotoxizität .
Eine im Projekt NanoCare durchgeführte 5 Tage Inhalations-Studie zeigte, dass eingeatmete Titandioxid-Partikel als Agglomerate in der Lunge deponiert werden, dann von Makrophagen aufgenommen werden und sich auch in lungenassoziierte Lymphknoten ablagern, wenn hohe Dosen verabreicht werden (50 mg/m3). Dagegen wurden in diesen Studien weder in der Leber, den Nieren, der Milz noch im Basalhirn mit anhängendem Riechkolben Nanopartikel nachgewiesen .
Ebenfalls im Rahmen des Projekts NanoCare vorgenommene Instillations-Studien mit niedriger (0,6 mg/Lunge) und hoher Dosis (4,8 mg/Lunge) zeigten eine geringfügige dosisabhängige Erhöhung der Anzahl an Makrophagen in der Lunge. Diese Zellen sind wichtig für die Immunabwehr und dienen der Beseitigung von Fremdstoffen, wie z.B. Partikel, durch Phagozytose.
In weiteren Instillations-Studien wurde gezeigt, dass sich Titandioxid-Partikel bei niedriger Dosierung in der Lunge ablagern und auch in die Leber und Nieren weitertransportiert werden können. Die geringen Mengen an Titandioxid hatten keine negativen Effekte auf die Lunge, führten jedoch zu einer vorübergehenden Veränderung der Metaboliten in der Leber und Niere. Im Gegensatz dazu wurde bei hohen Dosen eine starke Aggregation und Ablagerung von Partikeln in der Lunge beobachtet. Diese führte zu starken Entzündungsreaktionen. Ein Weitertransport von Titandioxid-Partikeln in Leber und Nieren wurde jedoch nicht nachgewiesen. Die Makrophagen konnten keine Phagozytose mehr vornehmen, somit war die Lunge mit Partikeln überladen .
Auch Kobayashi und Kollegen beschreiben in ihren Studien, dass Partikel in der Lunge Kurzzeiteffekte (24 h) verursachen können Die beobachteten Entzündungsreaktionen waren aber nach ca. 1 Monat wieder abgeklungen .
In 2021 hat die ECHA auf der Basis einiger Studien mit Hochdosisversuchen an Ratten die Klassifizierung von Titandioxid neu geregelt. Alltagsprodukte, die Titandioxid, egal in welcher Größe enthalten, müssen nach EUH212 wie folgt gekennzeichnet werden: „Achtung! Bei der Verwendung kann gefährlicher lungengängiger Staub entstehen. Staub nicht einatmen“. Der Europäische Gerichtshof erklärte jedoch die Verordnung der Kommission aus dem Jahr 2019 am 23. November 2022 für nichtig, soweit sie die harmonisierte Einstufung und Kennzeichnung von Titandioxid in bestimmten Pulverformen als karzinogener Stoff bei Einatmen betrifft. Das Gericht sagt in seinem Urteil, dass die Kommission einen Fehler bei der Beurteilung der Zuverlässigkeit und der Anerkennung der Studien begangen hat. Auf dieser fehlerhaften Bewertung beruhte die Einstufung.
Aufnahme über die Haut - Dermal
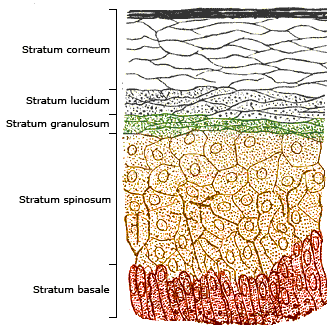
Zellschichten der menschlicher Oberhaut (Epidermis). © Wikipedia.de.
Titandioxid-Partikel werden nicht über die Haut in den Körper aufgenommen. Dies wurde u.a. im EU-Projekt NanoDerm für nano-Titandioxid-Partikel als Bestandteil von Kosmetika untersucht und bestätigt . Weitere Studien belegen dies durch Untersuchungen an der Schweinehaut, die der des Menschen sehr ähnlich ist . Aus Frankreich kommt eine weitere sehr gute Übersicht zur Sicherheit von Titandioxid-Partikeln in Sonnenschutzmitteln, die ebenfalls aus allen hinzugezogenen Studien keine Bedenken für den Einsatz von Titandioxid in Sonnenschutz herauslesen kann .
Um eine gute Dispersionseigenschaften der Sonnencreme zu erhalten, die Photostabilität zu gewährleisten und die Bildung von schädlichen sog. reaktiven Sauerstoffspezies (ROS) zu verhindern, werden die Titandioxid-Partikel außerdem beschichtet [siehe auch NanoDerm Schlussbericht, 2007].
Es bleibt die Frage zu klären, wie verletzte, entzündete oder besonders empfindliche Haut, wie beispielsweise durch Sonnenbrand geschädigte Haut, reagiert? Eine Studie aus dem Jahr 2011 konnte zeigen, dass Titandioxid- und Zinkoxid-Nanopartikel UVB geschädigte Haut (Sonnenbrand) ebenfalls nicht durchdringen können .
Die Partikel verbleiben in den oberen Schichten der Oberhaut (vgl. dazu den Artikel unter "Grundlagen - Wie werden innovative Materialien bzw. Nanomaterialien aufgenommen?").
Sonnencremes mit Titandioxid und Zinkoxid Nanopartikeln bieten wiederum einen effizienten Schutz gegen Hautschäden durch ultraviolettes Licht (UVB).
Aufnahme über den Magen-Darm-Trakt
Oral aufgenommene unlösliche mineralische Partikel werden meist über den Stuhl ausgeschieden. Bislang existieren jedoch nur wenige Analysen zu diesem Thema.
Studien mit behandelten Darmzellen des Menschen (20 und 80 µg/cm2) ergaben durchaus toxische Effekte nach 24-stündiger Behandlung. DNA-Schäden wurden allerdings nicht beobachtet . So wurde Titandioxid als Lebensmittelzusatzstoff E171 in 2008 zugelassen. Eine Neubewertung der Studien von 2015 bis 2020 durch die Europäische Agentur für Lebensmittelsicherheit (EFSA) in 2021 ergab jedoch ein anderes Bild . Durch die bestehenden Sicherheitsbedenken wurde Titandioxid im August 2022 in der EU als Lebensmittelzusatzstoff verboten (siehe dazu auch: https://germany.representation.ec.europa.eu/news/titandioxid-lebensmitteln-ab-sommer-2022-verboten-2022-01-14_de).
Wissenschaftlich bestehen Zweifel an diesem Verbot. So kommt die Gesundheitsbehörde in Kanada 2022 zu dem Schluss, dass es keinen Beleg für eine krebserzeugende Wirkung gibt. In Kanada bleibt Titandioxid in Lebensmitteln erlaubt (Health Canada, 2022). Auch in England ist man sich sicher, dass Titandioxid keine solche Wirkung hat und die Food Standards Agency (FSA) hat keinerlei Sicherheitsbedenken und Titandioxid bleibt ebenfalls dort erlaubt (COT, 2022).
Desweiteren haben internationale Expertengruppen Zweifel an der Evaluierung der EFSA und regen ein Überdenken dieser Entscheidung in der EU an .
Aufnahme über medizinische Anwendung
Titandioxid ist in sehr vielen Medikamenten als Füll- und Hilfsstoff enthalten. Ungeachtet des Verbotes in Lebensmitteln darf es weiterhin in Medikamenten eingesetzt werden, da keine Alternative zur Verfügung steht und ein sofortiges Verbot zu weiteren Engpässen bei der Medikamentenbereitstellung und -produktion führen würde. Allerdings hat die Europäische Medikamenten Agentur (European Medicines Agency, EMA) die Pharmaindustrie aufgefordert, möglichst rasch nach Alternativen zu suchen . Im April 2024 soll die EMA der EU einen Bericht dazu abgeben und die EU will danach weiter entscheiden, ob und wie Titandioxid weiter in Medikamenten genutzt werden darf (weitere Informationen der EMA). Die Mengen an Titandioxid in den einzelnen Tabletten oder anderen Darreichungsformen ist allerdings sehr gering. Keine der vielen Studien konnte bisher ein erkennbares Risiko solch niedriger Mengen an Titandioxid belegen.
Die Aufnahme von Titandioxid über Lebensmittel ist derzeit nicht gegeben, über Medikamente jedoch weiterhin möglich. Aus natürlichen Quellen wird jedoch Titandioxid auch über die Nahrung aufgenommen. Bisher konnte keine valide Studie ein Risiko durch oral aufgenommenes Titandioxid plausibel nachweisen. Über die Haut wird Titandioxid nicht aufgenommen. Über die Lunge kann Titandioxid vor allem aufgrund von Exposition am Arbeitsplatz aufgenommen werden. Die Risikobewertung dieses Materials ist allerdings seit einigen Jahren (2018 bis 2022) in der Diskussion. Weltweit wird Titandioxid sehr gegensätzlich reguliert.
Weitere Informationen
- NanoDermSchlussbericht (2007). Quality of Skin as a Barrier to ultra-fine Particles. QLK4-CT-2002-02678.
- Scientific Committee on Consumer Products (SCCP) (19.06.2007). Safety of nanomaterials in cosmetic products.
- EuGH (2022): Urteil des Europäischen Gerichtshofes. Download https://curia.europa.eu/jcms/upload/docs/application/pdf/2022-11/cp220190de.pdf
Die Wirkung von Titandioxid (TiO2) -Nanopartikeln wurde bereits in zahlreichen Pflanzen und Tieren untersucht. Damit gehören sie zu den am umfangreichsten getesteten Nanopartikeln. Es liegen in vivo und in vitro Daten vor und es wurden Experimente in verschiedenen Medien (Wasser, Boden) und mit verschiedenen Aufnahmewegen (Wasser, Nahrung, Blut, Boden) durchgeführt.
Allerdings sind die Studien nicht gut vergleichbar, weil sich die Partikel-Hersteller und damit in der Regel auch die Eigenschaften der Titandioxid-Partikel von Studie zu Studie unterscheiden [1].
 Die Regenbogenforelle als aquatischer Testorganismus ist besonders gut untersucht und wurde über Wasser, Nahrung und die Blutbahn mit Titandioxid-Nanopartikeln konfrontiert. In gröberer Form (mikroskalig) wird Titandioxid bereits seit langem in Ernährungsstudien in Fischen eingesetzt und gilt als untoxisch. Als Nanopartikel kann über die Nahrung aufgenommenes TiO2 in den Kiemen, im Darm, in der Leber, im Gehirn und in der Milz nachgewiesen werden. Es erfolgt also eine systemische Verteilung der Partikel im Körper, wobei dies keine Auswirkung auf die Gesundheit der Tiere hatte [2]. Direkt aus dem Wasser „verschluckte“ Titandioxid-Nanopartikel werden nur in geringem Maße in den Fischkörper aufgenommen [3].
Die Regenbogenforelle als aquatischer Testorganismus ist besonders gut untersucht und wurde über Wasser, Nahrung und die Blutbahn mit Titandioxid-Nanopartikeln konfrontiert. In gröberer Form (mikroskalig) wird Titandioxid bereits seit langem in Ernährungsstudien in Fischen eingesetzt und gilt als untoxisch. Als Nanopartikel kann über die Nahrung aufgenommenes TiO2 in den Kiemen, im Darm, in der Leber, im Gehirn und in der Milz nachgewiesen werden. Es erfolgt also eine systemische Verteilung der Partikel im Körper, wobei dies keine Auswirkung auf die Gesundheit der Tiere hatte [2]. Direkt aus dem Wasser „verschluckte“ Titandioxid-Nanopartikel werden nur in geringem Maße in den Fischkörper aufgenommen [3].
In einer weiteren Studie wurden Regenbogenforellen die TiO2-Nanopartikel direkt in die Blutbahn gespritzt (eine nicht umweltrelevante Exposition, die jedoch zur Klärung von Wirkmechanismen und Effekten bei Aufnahme sehr hoher Dosen dient, z.B. nach einem möglichen Industrieunfall) und die Verteilung in den Organen beobachtet [4]. Die Partikel reicherten sich in Nieren und Leber an, ohne jedoch die Funktionen dieser wichtigen Organe zu beeinflussen.
Zebrabärblinge können TiO2-Partikel ebenfalls aus dem Wasser aufnehmen. Die Eihülle der Fischembryonen ist jedoch für die Partikel nicht durchlässig. Werden Embryonen gegenüber den Partikeln bei gleichzeitiger starker Beleuchtung ausgesetzt, so treten Fehlbildungen auf und eine erhöhte Sterblichkeit der Embryonen wird beobachtet [5]. Dieser Effekt tritt bei normaler Beleuchtung nicht auf und ist somit auf die photokatalytischen Eigenschaften der TiO2-Partikel zurückzuführen. Erwachsene Zebrabärblinge zeigten keine Effekte nach TiO2-Exposition, die Kiemen wiesen keinerlei Veränderungen auf [6,7]. Es wurden jedoch Veränderungen in den Aktivitäten bestimmter Gene festgestellt, diese Genaktivitäten stimmten teilweise mit beobachteten Veränderungen nach Kupfer- und Silbernanopartikel-Exposition überein.
 Auch Wasserflöhe (Daphnien) zählen zu den häufig verwendeten Testorganismen. Im klassischen 2-Tages-Test, bei dem die Daphnien über 48 h mit den Partikeln exponiert werden, traten in verschiedenen Studien keine bzw. minimale Effekte (Beweglichkeit, Sterblichkeit) auf [6,8,9,10]. Wurde der Beobachtungszeitraum jedoch auf 3-21 Tage ausgedehnt, so traten Effekte auf die Häutung und die Fortpflanzungsfähigkeit auf, die z.T. zum Absterben aller Testorganismen führte [8,9,10]. Diese indirekten toxischen Effekte gehen einerseits auf eine Anheftung der Partikel an das Außenskelett (Panzer) der Tiere zurück, andererseits auf die Partikelaufnahme in den Darm [10]. Letztere behindert möglicherweise die Nahrungsaufnahme in den chronischen Tests.
Auch Wasserflöhe (Daphnien) zählen zu den häufig verwendeten Testorganismen. Im klassischen 2-Tages-Test, bei dem die Daphnien über 48 h mit den Partikeln exponiert werden, traten in verschiedenen Studien keine bzw. minimale Effekte (Beweglichkeit, Sterblichkeit) auf [6,8,9,10]. Wurde der Beobachtungszeitraum jedoch auf 3-21 Tage ausgedehnt, so traten Effekte auf die Häutung und die Fortpflanzungsfähigkeit auf, die z.T. zum Absterben aller Testorganismen führte [8,9,10]. Diese indirekten toxischen Effekte gehen einerseits auf eine Anheftung der Partikel an das Außenskelett (Panzer) der Tiere zurück, andererseits auf die Partikelaufnahme in den Darm [10]. Letztere behindert möglicherweise die Nahrungsaufnahme in den chronischen Tests.
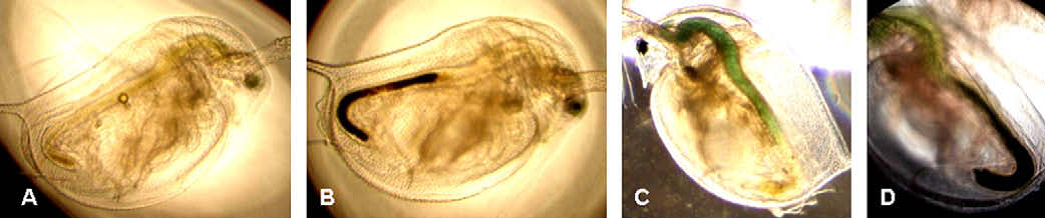
Wasserflöhe reichern Titandioxid-Nanopartikel im Darm an, erkennbar an der Schwarz-Färbung. © Zhu et al., 2010.
Eine wichtige Fragestellung in der Risikoforschung ist, inwieweit ein Transfer von Nanopartikeln über die Nahrungskette stattfindet. In einer `kleinen` Nahrungskette, bestehend aus Wasserflöhen und Zebrabärblinge, wurde gezeigt, dass eine Übertragung der Nanopartikel auf Zebrabärblinge, welche mit TiO2-exponierten Daphnien gefüttert wurden, stattfindet [11].
 Für weitere Süß- und Meerwasser-Organismen (Muscheln, Schnecken) waren Titandioxid-Nanopartikel nicht akut toxisch [12,13], jedoch zeigte die Aktivitäten bestimmter Enzyme eine Reaktion auf die Partikel-Exposition an [13,14].
Für weitere Süß- und Meerwasser-Organismen (Muscheln, Schnecken) waren Titandioxid-Nanopartikel nicht akut toxisch [12,13], jedoch zeigte die Aktivitäten bestimmter Enzyme eine Reaktion auf die Partikel-Exposition an [13,14].
 Der im Meeresboden lebende Wattwurm nahm keine Partikel über die Haut oder den Darm in Körpergewebe auf [15]. In sehr hohen Konzentrationen war die Futteraufnahme der Würmer verringert, eine typische Reaktion auf Verunreinigungen im Sediment. Ebenfalls in hohen Konzentrationen lösten TiO2-Nanopartikel hier DNA- und Zellschädigungen aus.
Der im Meeresboden lebende Wattwurm nahm keine Partikel über die Haut oder den Darm in Körpergewebe auf [15]. In sehr hohen Konzentrationen war die Futteraufnahme der Würmer verringert, eine typische Reaktion auf Verunreinigungen im Sediment. Ebenfalls in hohen Konzentrationen lösten TiO2-Nanopartikel hier DNA- und Zellschädigungen aus.
Als Beispiel für Boden-bewohnende Organismen wurden Kellerasseln mit Titandioxid-getränkten Blättern gefüttert. Die Nanopartikel hatten wenig Einfluss auf die Stoffwechselvorgänge und keinerlei Einfluss auf die Futteraufnahme, das Körpergewicht oder die Sterblichkeit [16,17], obwohl die eingesetzten Konzentrationen sehr hoch waren. Ähnlich wie für Wasserflöhe hatte eine verlängerte Expositionsdauer jedoch einen Einfluss auf die TiO2-Wirkung, ein Hinweis darauf, dass im Gegensatz den häufig angewandten Kurzzeittests auch chronische Test mit längeren Einwirkzeiten durchgeführt werden sollten. Eine Regenwurm-Art zeigte nach 7-tägiger TiO2-Exposition über den Boden DNA-Schädigungen und Hinweise auf oxidativen Stress, ebenfalls nur in sehr hohen Konzentrationen [18]. Ähnliche Befunde waren für den Fadenwurm zu beobachten, hier traten auch Verringerungen in Wachstum und der Zahl der Nachkommen auf [19].
 TiO2-Nanopartikel wurden an verschiedenen Pflanzen getestet, für die Zwiebel und Weidenbäume war die Toxizität gering, alle Wachstumsparameter waren unverändert [20,21]. Eine weitere Studie untersuchte Tabak- und Zwiebelpflanzen, hier zeigten hohe, nicht umweltrelevante Konzentrationen eine genotoxische Wirkung [22]. Für eine Süßwasser-Grünalge wurden für 3 verschiedene TiO2-Nanopartikel wachstumshemmende Effekte beobachtet, welche jedoch nicht allein durch unterschiedliche Partikelgrößen begründet werden können, sondern auch durch andere Eigenschaften wie unterschiedliche Kristallstrukturen [23]. Außerdem ist unklar, inwieweit die Nanopartikel den notwendigen Lichteinfall behindern und dadurch das Wachstum hemmen.
TiO2-Nanopartikel wurden an verschiedenen Pflanzen getestet, für die Zwiebel und Weidenbäume war die Toxizität gering, alle Wachstumsparameter waren unverändert [20,21]. Eine weitere Studie untersuchte Tabak- und Zwiebelpflanzen, hier zeigten hohe, nicht umweltrelevante Konzentrationen eine genotoxische Wirkung [22]. Für eine Süßwasser-Grünalge wurden für 3 verschiedene TiO2-Nanopartikel wachstumshemmende Effekte beobachtet, welche jedoch nicht allein durch unterschiedliche Partikelgrößen begründet werden können, sondern auch durch andere Eigenschaften wie unterschiedliche Kristallstrukturen [23]. Außerdem ist unklar, inwieweit die Nanopartikel den notwendigen Lichteinfall behindern und dadurch das Wachstum hemmen.
Als Fazit aus den bisher verfügbaren Studien lässt sich für Titandioxid-Nanopartikel eine geringe Toxizität für Umweltorganismen ableiten. Wirkungen wurden stets in Konzentrationen beobachtet, die weit über den vorhergesagten Umweltkonzentrationen liegen.
Die Partikel werden jedoch ohne Zweifel in Organismen und Zellen aufgenommen, weshalb man die wichtige Einschränkung machen muss, das die Wirkung von sehr geringen Konzentrationen dieser Stoffe über einen längeren Zeitraum, wie es den Verhältnissen in der Umwelt entsprechen würde, bisher nur unzureichend (in Daphnien und Kellerasseln) untersucht wurde.
Literatur
- Menard, A et al. (2011), Environ Pollut, 159(3): 677-684.
- Ramsden, CS et al. (2009), Ecotoxicology, 18(7): 939-951.
- Federici, G et al. (2007), Aquat Toxicol, 84(4): 415-430.
- Scown, TM et al. (2009), Toxicol Sci, 109(2): 372-380.
- Bar-Ilan, O et al. (2012), Nanotoxicology, 6(6): 670-679.
- Griffitt, RJ et al. (2008), Environ Toxicol Chem, 27(9): 1972-1978.
- Griffitt, RJ et al. (2009), Toxicol Sci, 107(2): 404-415.
- Dabrunz, A et al. (2011), PLoS One, 6(5): e20112.
- Wiench, K et al. (2009), Chemosphere, 76(10): 1356-1365.
- Zhu, X et al. (2010), Chemosphere, 78(3): 209-215.
- Zhu, X et al. (2010), Chemosphere, 79(9): 928-933.
- Canesi, L et al. (2010), Aquat Toxicol, 100(2): 168-177.
- Musee, N et al. (2010), Chemosphere, 81(10): 1196-1203.
- Canesi, L et al. (2010), Aquat Toxicol, 96(2): 151-158.
- Galloway, T et al. (2010), Environ Pollut, 158(5): 1748-1755.
- Drobne, D et al. (2009), Environ Pollut, 157(4): 1157-1164.
- Jemec, A et al. (2008), Environ Toxicol Chem, 27(9): 1904-1914.
- Hu, CW et al. (2010), Soil Biol Biochem, 42(4): 586-591.
- Wang, H et al. (2009), Environ Pollut, 157(4): 1171-1177.
- Klancnik, K et al. (2011), Ecotoxicol Environ Saf, 74(1): 85-92.
- Seeger, EM et al. (2008), J Soils Sediments, 9(1): 46-53.
- Ghosh, M et al. (2010), Chemosphere, 81(10): 1253-1262.
- Hartmann, NB et al. (2010), Toxicology, 269(2-3): 190-197.
Die Wirkung von Titandioxid Nanopartikeln wurde bereits in zahlreichen Pflanzen und Tieren untersucht. Damit gehören sie zu den am umfangreichsten getesteten Nanopartikeln. Es liegen in vivo und in vitro Daten vor und es wurden Experimente in verschiedenen Medien (Wasser, Boden) und mit verschiedenen Aufnahmewegen (Wasser, Nahrung, Blut, Boden) durchgeführt.
Verteilung und Wirkung im Körper
Bei den zuvor beschriebenen Effekten in der Lunge handelt es sich um akute Reaktionen. Über chronische Auswirkungen von nano-Titandioxid-Partikel auf den Körper liegen noch wenige Studien vor. Park und Kollegen schlossen aus ihren Untersuchungen, dass Titandioxid möglicherweise chronische Entzündungen der Lunge nach Instillation verursachen kann . Grundsätzlich wirken Titandioxid-Partikel entsprechend den granulären biopersistenten Staubpartikeln (GBS).
Nach der Neubeurteilung von Titandioxid durch die ECHA und die EFSA gab es Zweifel, ob Titandioxid nicht doch unter bestimmten Umständen eine tumorinduzierende Wirkung haben könnte und damit nicht sicher in seiner Verwendung ist. Der Europäische Gerichtshof hat im November 2022 die Regelung der ECHA als „zu Unrecht erlassen“ eingestuft [siehe auch Tagesschau-Meldung ]. Auch internationale Expertengruppen kamen nach ausführlicher Beurteilung der publizierten Daten zu der Überzeugung, dass es weder ausreichende Beweise für eine gesundheitsschädliche noch ein Indiz für eine mögliche karzinogene Wirkung des Titandioxid gibt .
Verhalten an der Blut-Hirn-Schranke
Das Gehirn ist durch die Blut-Hirn-Schranke sehr gut vor dem Eindringen von Fremdstoffen geschützt. Somit ist ein Endringen von Titandioxid-Partikeln unwahrscheinlich. Partikel könnten beim Einatmen über den Riechnerv direkt ins Hirn gelangen. In einer Studie an Ratten wurde gezeigt, dass nach der Injektion von Titandioxid-Nanopartikel in die Blutbahn keine Anreicherung der Partikel im Gehirn erfolgte . Weiterhin wurde nach dem Einflößen von Titandioxid in die Lungen von Mäusen kein Titan im Gehirn nachgewiesen .
Aufnahme und Wirkung in Zellen
Titandioxid-Partikel werden mehrheitlich als große intrazelluläre Aggregate in Vesikeln, Vakuolen oder Lamellarkörpern (membranumschlossene Zellbestandteile) mittels Phagozytose in die Zellen aufgenommen. Hohe Dosen stören jedoch die Phagozytose, so dass es zur Überladung der Zellen, z.B. in der Lunge kommt . Nur für kleine Aggregate (< 30nm) und einzelne Partikel wurde eine pinozytotische Aufnahme beobachtet. Nach der Aufnahme liegen die Titandioxid-Partikel meist membrangebunden im Zytoplasma der Zellen vor. Es wurden bisher keine Partikel im Zellkern gefunden .
In vitro Mehrfachzellsysteme (auch Kokultursysteme genannt) simulieren das Zusammenspiel verschiedener Zellen im Körper und damit die in vivo Situation besser als einfache Zellkulturmodelle mit nur einem Zelltyp. Mittels sensibler Methoden konnte gezeigt werden, dass Titandioxid in allen Zelltypen eines 3-fach Kokultursystems als membrangebundene größere Aggregate, aber auch frei im Zytoplasma als kleinere Aggregate oder einzelne Partikel vorliegen .
Die Transzytose, also die Weitergabe von einer Zelle zur anderen, ist dagegen in vitro kaum untersucht. Messungen im Rahmen des Projektes NanoCare zum Transport von Nanopartikeln durch Zellen ergaben, dass kein Transport von Titandioxid-Partikel durch einlagige Zellschichten stattfindet . Exozytose, ein Vorgang, bei dem Stoffe aus der Zelle an die Zellumgebung abgegeben werden, konnte in in vitro Versuchen nicht beobachtet werden.
Zahlreiche in vitro Studien mit unterschiedlichen Zellen zeigen, dass Zellen je nach Typ und Herkunft verschieden stark auf eine Exposition mit Titandioxid reagieren. In Abhängigkeit von der Dosis können Titandioxid Nanopartikel die Sekretion von Entzündungsmarkern, die Bildung von reaktiven Sauerstoffspezies (ROS), Zytotoxizität und Apoptose hervorrufen .
Es sind jedoch sehr hohe Konzentrationen an nanoskaligem Titandioxid (15 nm Primärpartikelgröße) notwendig, um die Zellen unwiederbringlich zu schädigen .
In Studien mit menschlichen Nasenschleimhautzellen und weißen Blutkörperchen wurden jedoch keine Zell- bzw. DNA-Schädigungen nachgewiesen, obschon vereinzelt Partikel und vermehrt auch Agglomerate in den Zellen vorhanden waren .
Im Projekt NanoCare diente Titandioxid als sog. „Referenzmaterial“, d.h. es wurde in allen Versuchen mitgeführt. Untersuchungen mit unterschiedlichen Zelllinien zeigten, dass verschiedene Varianten von Titandioxid nur nach Gabe sehr hoher Dosen (50 µg/cm2) die Vitalität der Zellen reduzierte. Diese Dosis liegt nicht nur weit über der Menge an natürlich vorhandenem Titandioxid, sondern auch über derjenigen, die durch sachgemäßen Gebrauch von industriell hergestelltem Titandioxid entsteht. Zudem neigt Titandioxid zu starker Verklumpung, was die Menge an freien Nanopartikeln stark reduziert .
Mit Hilfe des sogenannten Vektor-Modells, das einige der elementaren Zellfunktionen abbildet , konnte gezeigt werden, dass eine Konzentration von ca. 60 µg Partikeln pro 106 Fresszellen zu einer Schädigung der Zellen führt. Auch die Bildung von reaktiven Sauerstoffspezies (ROS) wurde erst bei dieser hohen Dosis in den Zellen detektiert .
Im Rahmen des Projekts NanoCare wurden in vitro Tests auch mittels eines am KIT entwickelten Expositionssystems für Bioassays zur Bestimmung der Toxizität gasgetragener Nanopartikel durchgeführt. Aerosol strömt hierbei über die Oberfläche von Zellen und kann durch die deponierten Partikel eine dosisabhängige Reaktion in den Zellen, wie zum Beispiel Entzündung, hervorrufen. Gleichzeitig wird die deponierte Partikeldosis pro Fläche mit einer Schwingquarzmikrowaage aufgezeichnet (siehe KIT-Flyer).
Im BMBF geförderten Verbundprojekt INOS wurde Titandioxid ebenfalls als Referenzmaterial eingesetzt. In den in vitro Tests zeigte sich übereinstimmend, dass Titandioxid auf verschiedene humane Zelllinien (A549, HaCaT, CaCo-2) und auch auf Zellen der Regenbogenforelle keine zytotoxische Wirkung zeigte (eingesetzte Konzentrationen bis 50 µg/ml über 3 Stunden und 3 Tage) [siehe dazu auch die INOS Forschungsberichte, 2009].
Grundsätzlich zeigen die meisten Studien keine gesundheitsschädlichen Wirkungen durch Titandioxid. Allerdings wurden in den vergangenen 10 Jahren vermehrt Studien mit sehr hohen Konzentrationen durchgeführt. Diese und Hochdosisstudien aus den 90er Jahren des letzten Jahrhunderts führten dazu, dass die Französische Agentur für Nahrungssicherheit, Umwelt und Arbeitsschutz (ANSES) einen Antrag bei der Europäischen Chemikalien Agentur ECHA stellte, Titandioxid neu einzustufen. Die ECHA folgte diesem Antrag und führte eine neue Kennzeichnung aller Titandioxid enthaltenden Produkte ein. Die Europäische Behörde für Lebensmittelsicherheit EFSA verbot daraufhin die Verwendung von Titandioxid in Lebensmitteln. Der Europäische Gerichtshof hat die Kennzeichnungspflicht aufgrund fehlender Indizien wieder aufgehoben. Weitere Entscheidungen sind zukünftig zu erwarten.
Weiterführende Informationen:
- INOS Forschungsberichte (siehe Veröffentlichungen des Projekts INOS)
- KIT Flyer (https://nanopartikel.info/wissen/materialien/titandioxid/files/wissensbasis/titandioxid/Karlsruher-Expositionssystem-Datenblatt.pdf )
- EuGH (2022): Urteil des Europäischen Gerichtshofes. Download https://curia.europa.eu/jcms/upload/docs/application/pdf/2022-11/cp220190de.pdf
Generell wird davon ausgegangen, dass sich Titandioxid -Partikel (unabhängig von ihrer Größe) nicht auflösen, somit ist von einem Verbleib des TiO2 in partikulärer Form in der Umwelt auszugehen. Studien zum Umweltverhalten von TiO2Nanopartikeln wurden unter drei Hauptaspekten durchgeführt: Einfluss von Umweltbedingungen auf das Vorliegen und die Mobilität der Partikel, Bindung von Umweltkontaminanten durch die Partikel und Einfluss der Partikel auf Prozesse in der Umwelt.
Studien zum Einfluss von Umweltbedingungen auf die Mobilität beschäftigen sich insbesondere mit natürlich in Boden oder Wasser vorkommenden Substanzen und ihrer Interaktion mit den Nanopartikeln. Dabei geht es besonders um den Einfluss auf die Agglomeration, sowie die Stabilität und Ablagerung der Partikel. Zu den natürlichen Stoffen gehören organische Materialien (Abbauprodukte von Pflanzen oder Tieren), wie Humin- oder Fulvinsäuren, welche in allen Gewässern und Böden zu unterschiedlichen Anteilen enthalten sind.
In den meisten Fällen führt eine Bindung solcher Materialien an TiO2 zu einer Stabilisierung der Partikelsuspension und verhindert deren Agglomeration [1-7]. Das führt dazu, dass Partikel eher im Wasser „schweben“, dadurch beweglich bleiben und nicht absinken. Die Stabilisierung durch organische Materialien erfolgt weitgehend unabhängig von pH-Wert und Salzgehalt der Umgebung, d.h. unter verschiedensten Umweltbedingungen. Proteine haben einen den organischen Materialien vergleichbaren Effekt, indem sie eine Agglomeration ebenfalls wirksam verhindern [8].
Bestimmte Substanzen (organische Säuren, z.B. Oxalsäure) können jedoch auch gegenteilige Effekte haben bzw. keinen stabilisierenden Einfluss ausüben [9]. Mineralien oder Salze erhöhen ebenfalls die Agglomeration der Partikel [10] und verringern ihre Beweglichkeit [1].
Das Verhalten der Partikel wird auch von den chemischen und physikalischen Eigenschaften beeinflusst. So können Verunreinigungen (z.B. Rückstände aus der Herstellung) einen Einfluss auf die Oberflächenladung und damit das Verhalten der Partikel haben [11,5]. Die verschiedenen kristallinen Strukturen des TiO2 bzw. verschiedene Formen und Größen hingegen haben laut den vorliegenden Studien keinen Einfluss auf Sedimentation und Agglomeration der Partikel.
Neben den natürlichen organischen Stoffen können auch anorganische Stoffe an Titandioxid-Partikel binden und dadurch ihr Verhalten in der Umwelt und ihre Wirkung auf Umweltorganismen beeinflussen. Titandioxid-Partikel können giftige Schwermetalle wie Cadmium und Arsen binden [12,13,14].
Karpfen, die Cadmium- bzw. Arsen-haltigem Wasser mit Titandioxidpartikeln ausgesetzt waren, nahmen mehr Cadmium und Arsen auf als Karpfen in partikelfreiem Wasser [13,14]. Bei Algen hingegen war dieser Effekt nicht zu beobachten, weil Algen die Cadmium-beladenen Partikel nicht aufnehmen [12]. Arsen wird durch die photokatalytische Wirkung des TiO2 in eine weniger giftige Form umgewandelt [15]. Ebenso wurde eine erhöhte Bindung von Phosphor an TiO2 beschrieben [16].
Somit können TiO2-Nanopartikel prinzipiell zahlreiche Stoffe binden und die Verfügbarkeit für Organismen erhöhen. Ob TiO2 auch unter Freilandbedingungen einen signifikanten Einfluss auf die Verfügbarkeit anderer Schadstoffe hat, wurde noch nicht untersucht.
TiO2-Nanopartikel können auch Einfluss auf Prozesse in der Umwelt nehmen, indem sie beispielsweise die Eigenschaften von Sedimenten hinsichtlich Oberfläche, Porengröße und Bindungsfähigkeit für andere Stoffe verändern [16]. Auswirkungen könnten z.B. eine erhöhte Bindung von Nährstoffen in TiO2 belasteten Böden sein, genauere Folgen einer TiO2-Anreichung sind jedoch noch unerforscht.
Auch Wasserreinigungs-Prozesse in Kläranlagen können durch hohe TiO2-Konzentrationen beeinflusst werden. So sind Auswirkungen auf die Entfernung von Stickstoffverbindungen beschrieben [17] .
Literatur
- Ben-Moshe, T et al. (2010), Chemosphere, 81(3): 387-393.
- Domingos, RF et al. (2009), Environ Sci Technol, 43(5): 1282-1286.
- Keller, AA et al. (2010), Environ Sci Technol, 44(6): 1962-1967.
- Thio, BJ et al. (2011), J Hazard Mater, 189(1-2): 556-563.
- Von Der Kammer, F et al. (2010), Environ Pollut, 158(12): 3472-3481.
- Yang, K et al. (2009), Langmuir, 25(6): 3571-3576.
- Zhang, Y et al. (2009), Water Res, 43(17): 4249-4257.
- Allouni, ZE et al. (2009), Colloids Surf B Biointerfaces, 68(1): 83-87.
- Pettibone, JM et al. (2008), Langmuir, 24(13): 6659-6667.
- French, RA et al. (2009), Environ Sci Technol, 43(5): 1354-1359.
- Liu, X et al. (2011), J Colloid Interface Sci, 363(1): 84-91.
- Hartmann, NB et al. (2010), Toxicology, 269(2-3): 190-197.
- Sun, H et al. (2009), Environ Pollut, 157(4): 1165-1170.
- Zhang, X et al. (2007), Chemosphere, 67(1): 160-166.
- Pena, ME et al. (2005), Water Res, 39(11): 2327-2337.
- Luo, Z et al. (2011), J Hazard Mater, 192(3): 1364-1369.
- Zheng, X et al. (2011), Environ Sci Technol, 45(17): 7284-7290.
 >
>