In vitro Tests kommen in vielen Gebieten der Biowissenschaften im Einsatz, weil sie meist schnell und relativ kostengünstig durchführbar sind. Man versteht darunter die Untersuchung biologischer Vorgänge außerhalb eines Organismus. Vor allem bei der Entwicklung von Medikamenten kommen sie zum Einsatz. Doch neben all ihrer Vorzüge hat ihre Verwendbarkeit und Aussagekraft, speziell in der Nanosicherheit, Grenzen, da Nanopartikel aufgrund ihrer einzigartigen Eigenschaften diese Methoden behindern können.
In der Forschung zur Nanosicherheit werden überwiegend menschliche Zellen verwendet. Es handelt sich dabei entweder um Zellen, die Menschen entnommen wurden, oder um im Labor kultivierte Zell-Linien, die von Krebszellen oder virusinfizierten Zellen abstammen und die sich beliebig vermehren lassen. Die Bedingungen für in vitro Tests lassen sich sehr gut kontrollieren und es ist in der Regel möglich, eine größere Anzahl von Versuchen durchzuführen als mit Tierversuchen. Es gibt für sie auch nicht die gleichen ethischen Probleme, obwohl auch hier beispielsweise bei der Verwendung von Patientenmaterial oder Stammzellen entsprechende Richtlinien einzuhalten sind. Man kann für einen Test auch unterschiedliche Zellen aus verschiedenen Organsystemen in sogenannten Ko-Kulturen kombinieren, und damit auch in gewissem Umfang Organstrukturen nachbilden. Es können aber unter Umständen auch Organteile oder Organe für solche Untersuchungen verwendet werden, wie das Beispiel der menschlichen Plazenta zeigt [1].
Welche Tests gibt es?
Es sind zahlreiche Testverfahren in der wissenschaftlichen Literatur beschrieben, die für unterschiedliche Anwendungen entwickelt wurden. Die Bandbreite ist dabei sehr groß und reicht von einfachen Zellkultursystemen mit nur einer leicht vermehrbaren Zellsorte bis zu hochkomplexen Ko-Kultur-Systemen („Organ-on-chip“, „Body-on-chip“) mit mehreren Zelltypen, die aus Patientenmaterial für jeden Test frisch gewonnen werden müssen oder für die zuvor reprogrammierte Stammzellen erzeugt werden müssen (sogenannte induzierte pluripotente Stammzellen, iPS Zellen). Auch gibt es eine Vielzahl an Tests, die für verschiedenste Fragestellungen entwickelt wurden und mit denen man ebenso viele unterschiedliche Parameter messen kann (sogenannte Endpunkte). Tests mit beliebig vermehrbaren Zellen sind besonders schnell und preisgünstig durchzuführen. Die Vitalität von Zellen lässt sich dabei etwa durch einem einfachen Farbtest bestimmen, z.B. dem MTT Test. Im COMET Test liefern Fluorenzenzsignale Hinweise auf DNA-Schädigung.
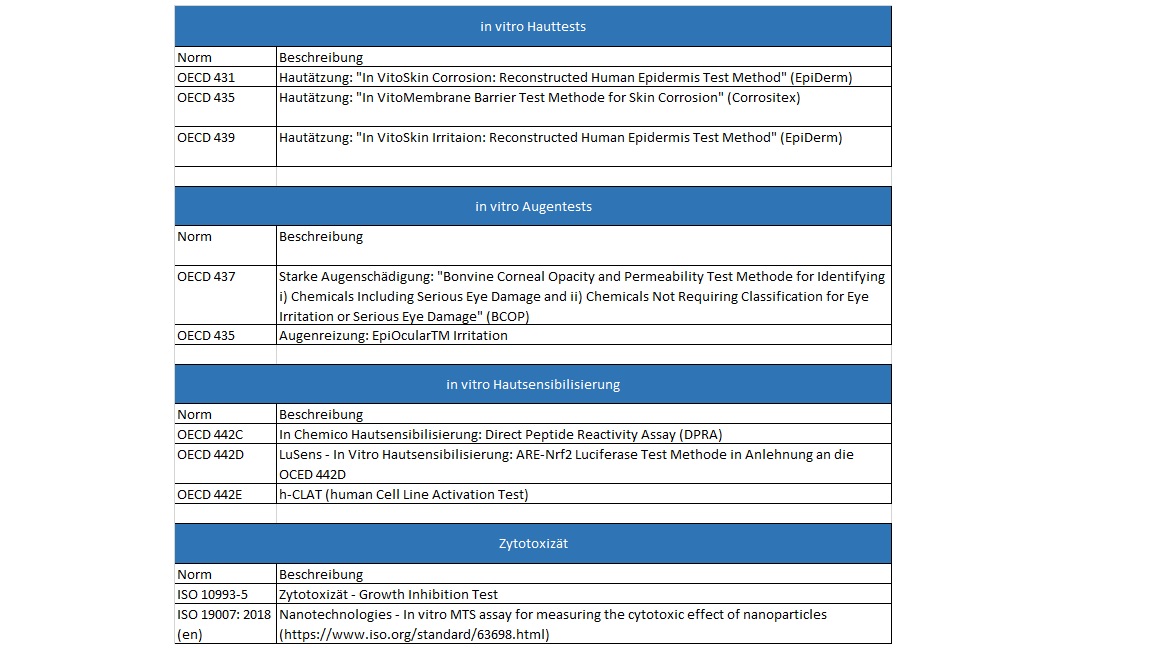
Die Organisation für wirtschaftliche Zusammenarbeit und Entwicklung (OECD) führt eine Liste von derzeit etwa 150 Tests für Chemikalien [2]. Dieses Verzeichnis international anerkannter Verfahren enthält unter anderem Tests für DNA Schädigung, Augenirritation, Neurotoxizität, Sensibilisierung der Haut, Fortpflanzungsstörungen und Effekte bei Einatmen oder Verschlucken.
Für den Nachweis der Sicherheit von Nanomaterialien ist es wichtig, dass solche Tests von unabhängigen Stellen anerkannt werden. Klassische in vitro Tests sind teilweise direkt für Nanomaterialien anwendbar, in manchen Fällen braucht man jedoch geänderte Verfahren, um den speziellen Eigenschaften von Nanopartikeln gerecht zu werden (siehe Tabelle). Viele Partikel sind zum Bespiel farbig oder lichtundurchlässig (z.B. Carbon Black). Das ist eine wesentliche Einschränkung, da viele Systeme Nachweise mit Hilfe von Licht erzielen. Inzwischen sind ältere Methoden für die Verwendung mit Partikeln angepasst worden und neue Methoden wurden speziell für Partikel entwickelt. Die weitere Entwicklung und Zertifizierung solcher Tests ist ein aktives Forschungsgebiet.
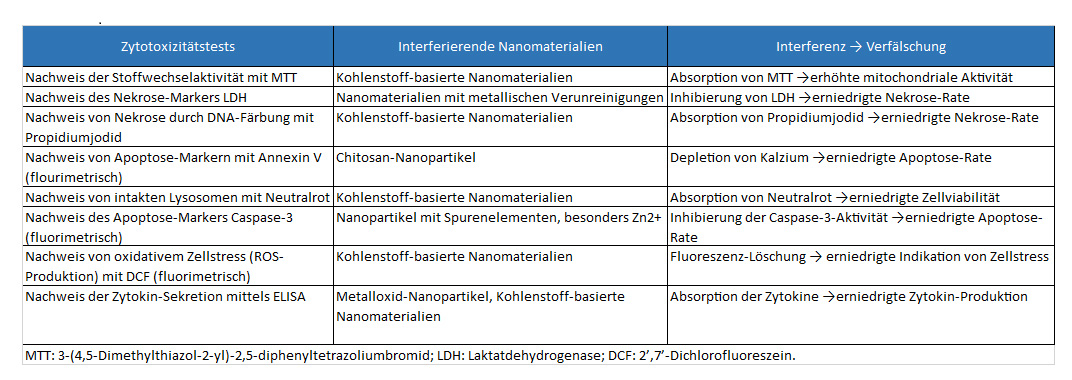
In Vitro Test Interferenzen (Quelle Kroll et al. (2010): Biospektrum 01/2010:48-50)
Wer führt solche Tests durch?

Frau im Labor © sergiophoto / Fotolia.com
In vitro Tests sind in vielen Gebieten der Biowissenschaften im Einsatz wie z.B. in der Medizin, Biomedizin, Pharmazie, Biochemie, Molekularbiologie, Chemie und Toxikologie. In all diesen Gebieten befasst man sich mit dem Verhalten von Zellen und/oder mit der Wirkung von Substanzen oder Umwelteinflüssen auf Zellen und Organsysteme.
Ihre wichtigste Verwendung in der angewandten Forschung haben in vitro Tests in der Entwicklung von Medikamenten, wo sie von der Pharmaindustrie in großem Maßstab verwendet werden. Untersuchungen zu den biologischen Wirkungen von Nanomaterialien stützen sich dabei überwiegend auf Methoden, die für die Grundlagen- und Pharmaforschung entwickelt wurden. Wie oben bereits erwähnt, wurden einige dieser Methoden speziell für die Anwendung mit Nanopartikeln geprüft und ggf. weiterentwickelt. Untersuchungen mit Nanopartikeln greifen daher heute auf eine Palette von geeigneten Methoden zurück, die von Forschungseinrichtungen und Firmen verwendet werden – auch von Pharmafirmen, die wegen der zunehmenden Verwendung von Nanopartikeln in der Nanomedizin großes Interesse daran haben.
Wie sind die Möglichkeiten und Grenzen solcher Tests?
In der Pharmaindustrie wird bei der Entwicklung von Medikamenten eine Kombination von in vitro Tests und Tierversuchen verwendet. Dies wird von den Genehmigungsbehörden verlangt, um das Risiko für die Testpersonen in den ersten Versuchen einer Medikamentenstudie am Menschen möglichst gering zu halten. In vitro Tests sind sehr nützlich. Aber es gibt auch Fragestellungen, die nur an Tieren zu untersuchen sind, die über einen ähnlich komplexen Organismus wie wir Menschen verfügen und in denen ein vergleichbares Krankheitsbild vorliegen kann wie beim Menschen.
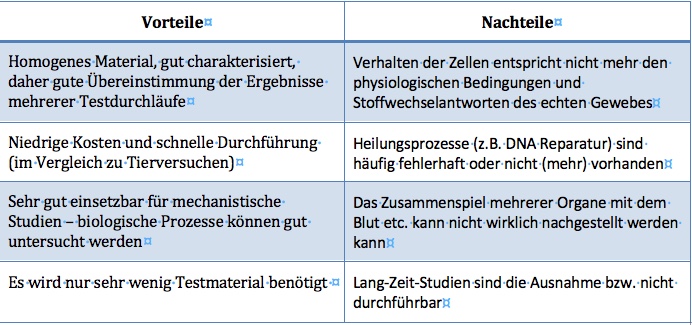
Vor-und Nachteile von in vitro Tests (Quelle: H. F. Krug)
Ein wesentlicher Vorteil von in vitro Tests ist, dass sie oft relativ schnell und preisgünstig sind, so dass große Probenzahlen bewältigt werden können. Man kann mit menschlichen Zellen arbeiten, ist also in der Spezies, die uns gewöhnlich am meisten interessiert. Es sind Zellen aus vielen unterschiedlichen Organen verfügbar, so dass man meist Daten zu dem Gewebe gewinnen kann, das gerade wichtig ist. In Zellkultur kann man die Bedingungen sehr gut kontrollieren und manipulieren, was etwa für die Aufklärung von molekularen Mechanismen sehr wichtig ist. Manche Zellen stammen von Organen oder Organteilen von freiwilligen Spendern, die bei medizinischen Eingriffen entnommen wurden. Häufig weisen diese Merkmale des Krankheitsbildes des Patienten auf, so dass mit Hilfe der gewonnenen Zellen aus dem geschädigten Gewebe sogar Aspekte von Krankheitszuständen recht realistisch im Labor nachgebildet werden können.
Die Methodik hat ihre Einschränkungen, denn eine einzelne Lungenzelle z.B. kriegt kein Asthma. Man kann bestimmte Aspekte simulieren, man kann auch dreidimensionale Modelle aus unterschiedlichen Zelltypen herstellen, aber es ist schlussendlich keine intakte Lunge. Forscher bemühen sich, organartige Strukturen („Organoide“) aus Stammzellen herzustellen, aber auch das ist nur eine Annäherung und überdies für Routineanwendungen bisher zu schwierig. Dazu kommt, dass Zell-Linien, die aus Tumoren gewonnen wurden, genetisch verändert sind. Das heißt, dass sie sich unbegrenzt teilen können und so für die Forscher in großer Zahl und über einen langen Zeitraum zur Verfügung stehen. Sie entsprechen somit aber nicht wirklich den Zellen des Originalgewebes. Frisch aus dem Menschen entnommene Zellen entsprechen zwar eher der realen Situation, es gibt aber oft große Unterschiede von Person zu Person. Auch verändern diese frischen Zellen von Patienten in der künstlichen Umgebung eines Labors sehr rasch ihre spezifischen Eigenschaften, so dass man keine völlig verlässlichen Ergebnisse aus den Untersuchungen ziehen kann. Manche Zellen sind einfach zu gewinnen, etwa aus dem Blut; andere sind dagegen kaum zugänglich, etwa aus dem Gehirn.
Die Zukunft
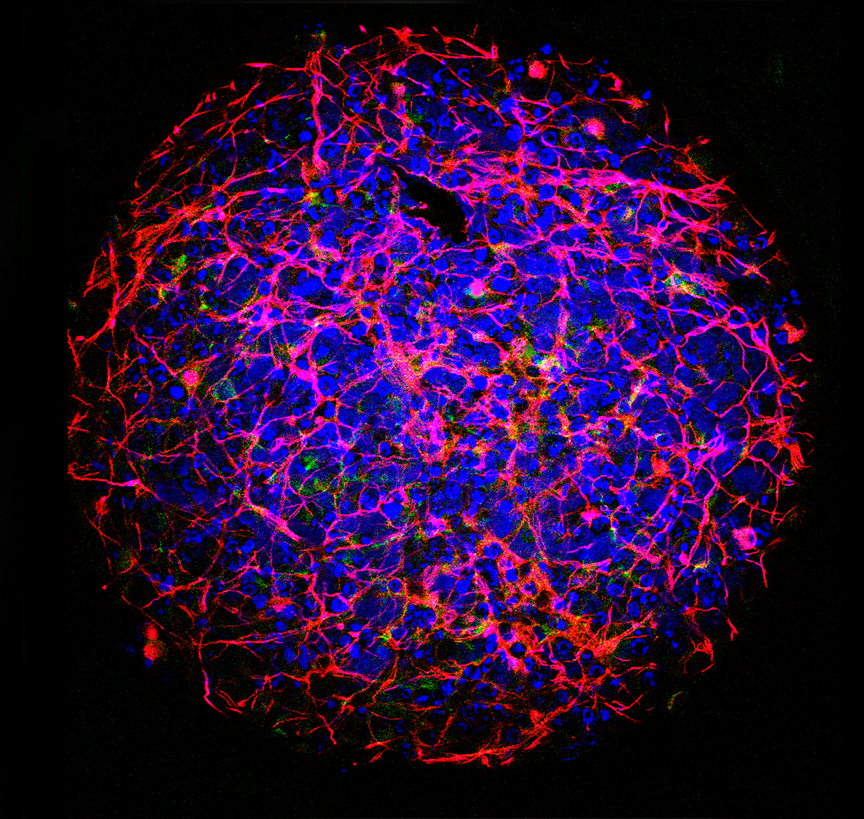
Mikroskopiebild eines kugelförmigen „Minigehirns“ (ca.0.5 mm Durchmesser), aus Neuronen und weiteren Zelltypen im Labor erzeugt. ©CAAT, JOHNS HOPKINS Bloomberg School of Public Health
Es ist derzeit eine Herausforderung, Tests immer noch einfacher und preisgünstiger zu gestalten, ohne dass ihre Zuverlässigkeit abnimmt. Es wird erwartet, dass die großen Zukunftsthemen Automatisierung und Digitalisierung auch auf diese Entwicklungen einen großen Einfluss haben werden. Schon heute existieren an Forschungseinrichtungen und in Firmen Methodenplattformen, mit denen einfache in vitro Wirkstofftests im Hochdurchsatzverfahren mit Hilfe von Robotern durchgeführt werden können. Ideal wären Methoden, die z.B. direkt in einer Fabrikhalle automatisiert angewendet werden könnten, so dass die Arbeitsplatzsicherheit mit biologischen Methoden online überwacht werden kann. Mit standardisierten in vitro Testverfahren könnte man also die Sicherheit von Produkten aber auch die Arbeitsplatzsicherheit gewährleisten. Aber es gilt der Grundsatz, dass diese Verfahren von den Behörden akzeptiert und zugelassen werden müssen.
In vitro Testverfahren sind seit Jahrzehnten im Gespräch, Tierversuche möglichst ganz zu ersetzen. Bereits 1959 haben M.S. Russell and R.L. Burch das visionäre 3R-Prinzip entwickelt: Replacement, Reduction, Refinement, was so viel bedeutet wie: Ersetzen, Reduzieren, Verbessern (Tierleid mindern). Um dieses Ziel aber wirklich erreichen zu können, ist ein weiteres Problem zu überwinden. Zellen in einer Petrischale verhalten sich nicht wie in ihrer originalen Umgebung im Organ, da ihnen wichtige Zell-Zell-Kontakte fehlen. Aus diesem Grund ist die Tendenz in der modernen Zellbiologie mit in vitro Organmodellen diese Kontakte auch im Labor nachzustellen (siehe Bild des „Minigehirns“ unten). Diese komplexen in vitro Modelle werden zurzeit in speziellen Forschungsprogrammen weiterentwickelt, um zukünftig in der Grundlagen- und Pharmaforschung ganz oder teilweise auf Tierversuche verzichten zu können.
Literatur
- Grafmüller,S. et al., (2013). J. Vis. Exp. 76: e50401
- OECD Guidelines for the Testing of Chemicals, Section 4, Health Effects, ISSN: 2074-5788 (online)
 >
>