Ein Großteil des natürlichen Bariumsulfats wird bei der Erdöl- und Erdgasförderung verwendet. Als sogenannter Bohrspat erhöht das Mineral die Dichte des Bohrschlamms, so dass Gesteinsbrocken darin frei treiben können, ohne das Bohrloch zu verstopfen. Es dient zudem als Füllstoff und Additiv bei einigen hochwertigen technischen Produkten, wie beispielsweise bei Brems- und Kupplungsbelägen oder auch Teppichbeschichtungen. Verwendet wird es außerdem als Röntgenkontrastmittel und Knochenzement. Meist liegt es hier als Mischung aus Nano- und Mikropartikeln vor. Künstlich hergestelltes Bariumsulfat wird Permantweiß genannt und hauptsächlich für Anstrichstoffe verwendet (Grundierungen und Füller bei Automobillackierung, Industrielacken, Bauten-, Holz- sowie Druckfarben).
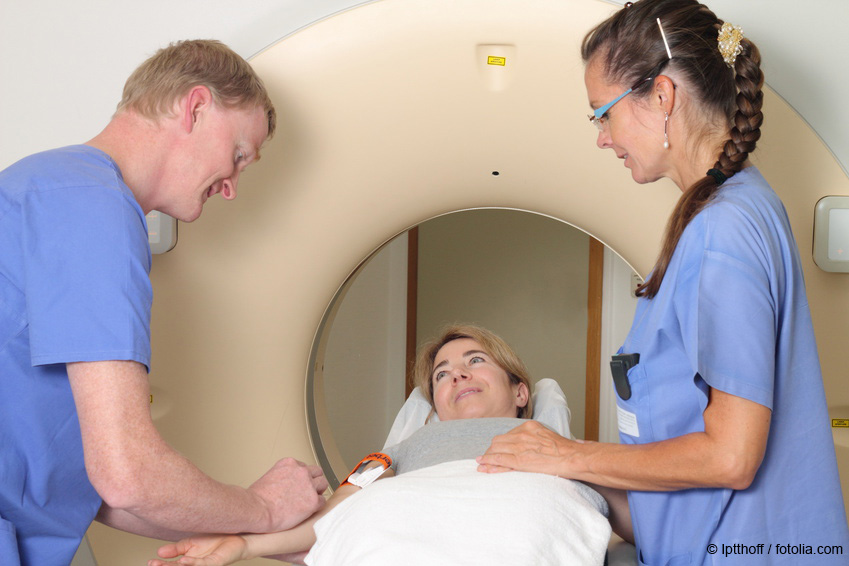
Radiologe gibt Kontrastmittell ©potthoff / fotolia.com
Wie könnte ich damit in Kontakt kommen?
Bariumsulfat dient hauptsächlich als Füllstoff bei der Herstellung technischer Produkte, so dass Verbraucher selten direkt mit der Substanz in Kontakt kommen. Anders ist dies bei der medizinischen Anwendung als Röntgenkontrastmittel oder Knochenzement: Hier wird den Patienten Bariumsulfat gezielt verabreicht.
Wie gefährlich ist das Material für Mensch und Umwelt?
Kontrastmittel auf Basis von Bariumsulfat wird vom Magen-Darm-Trakt nicht aufgenommen. Es eignet sich deshalb hervorragend dazu, bei Röntgenuntersuchungen die Form des Verdauungstraktes hervorzuheben. Anschließend wird es unverändert wieder ausgeschieden. Ebenfalls ist erwiesen, dass eingeatmete Bariumsulfat-Partikel sich nicht in der Lunge ablagern und somit keine schädlichen Effekte hervorrufen. Auch die Blut-Hirn-Schranke durchdringt Bariumsulfat nicht.
Derzeit sind keine Daten dazu vorhanden, wie Nanopartikel aus Bariumsulfat sich in der Umwelt verhalten.
Fazit
Im Alltag sind der menschliche Körper und die Umwelt nur geringen Mengen an nanoskaligem Bariumsulfat ausgesetzt. Im Fall der medizinischen Anwendungen ist erwiesen, dass Nanopartikel aus Bariumsulfat keinen schädlichen Effekt auf den menschlichen Körper haben.
Nebenbei
- Weil Bariumsulfat besonders gut Gamma- und Röntgenstrahlung absorbiert, eignet es sich in Verbindung mit Beton auch als Abschirmmaterial für Atomenergieanlagen.
- Die wichtigsten Lagerstätten für Bariumsulfat in Deutschland befinden sich bei Meggen in Westfalen
Eigenschaften und Anwendungen

Baryt © M.Dorr & M.Frommherz / Fotolia.com
Bariumsulfat (BaSO4) ist das Barium-Salz der Schwefelsäure. Der Name Barium leitet sich vom griechischen barys (schwer) ab, was von dem hohen Atomgewicht des Barium (M=137) herrührt.
Die wichtigsten Kennzeichen von Bariumsulfat, die auch seine technische Bedeutung bestimmen, sind die hohe Dichte, die chemische Inertheit, das Reflexionsvermögen von elektromagnetischer Strahlung und der perlmutartige Glanz sowie eine geringe Löslichkeit in Flüssigkeiten und eine geringe Ölaufnahme. Die Dichte von natürlichem Bariumsulfat beträgt 4,3-4,6 g/cm³. In Wasser, Säuren und Laugen ist Bariumsulfat praktisch unlöslich (Ausnahme: heiße konzentrierte Schwefelsäure). Bariumsulfat ist infolge seiner äußerst geringen Wasserlöslichkeit im Gegensatz zu anderen Barium-Verbindungen ungiftig
Die Hauptmenge des natürlichen Bariumsulfats wird bei der Erdölförderung und Erdgasförderung zur Erzielung eines Bohrschlammes hoher Dichte eingesetzt (Bohrspat), der die Bohrlöcher durch Flotation von Gesteinsbrocken frei hält.
Natürliches Bariumsulfat kann aufgrund seiner hohen Reinheit aber ohne größere Aufbereitung auch zur Herstellung hochwertiger Produkte dienen. Als Füllstoff findet es sowohl in der Kunststoffindustrie als auch in der Lack- und Farbenindustrie Verwendung (Füllstoffspat). In Kunststoffen verbessert Bariumsulfat die Verarbeitbarkeit und erhöht das Gewicht, was die schalldämmende Wirkung von Kraftfahrzeugfußmatten, Teppichbeschichtungen oder Kunststoffabwasserrohren erhöht. Die chemische Inertheit und hohe Temperaturstabilität wird in Kupplungsbelägen oder Bremsbelägen ausgenutzt, in denen bis zu 40% Bariumsulfat enthalten sind. In der Lack- und Farbenindustrie dient BaSO4 neben der Volumengebung vor allem zur Verbesserung der Verarbeitungseigenschaften. Wichtige Anwendungsgebiete sind Spachtelmassen, Füller und Grundierungen. In der Textilindustrie dient Bariumsulfat als Weißwaren-Appretur, zum Mattieren von Viskose im Druck und im Weißätzen. Aufgrund seines hohen Absorptionskoeffizienten für Gamma- und Röntgenstrahlung eignet es sich in Verbindung mit Beton (Barytbeton, Barytzement) auch als Abschirmmaterial für Atomenergieanlagen. Auch in zahlreichen Röntgenkontrastmitteln ist Bariumsulfat (Röntgenbaryt) enthalten.
Etwa 70% des synthetischen Bariumsulfats Blanc fixe (Permanentweiß) werden für Anstrichstoffe verwendet. Neben der verglichen mit Baryt größeren Helligkeit ist hier vor allem die gezielt einstellbare Teilchengröße von Vorteil. Wichtige Anwendungen sind Grundierungen und Füller bei Automobillackierung, Industrielacken, Bauten-, Holz- sowie Druckfarben. In Decklacken wird es als "Spacer" zur Verbesserung der Streueigenschaften von Titandioxid Pigmenten eingesetzt oder zur Verhinderung der Flockulation organischer oder anorganischer Buntpigmente eingesetzt. Bei der Verwendung zusammen mit Zinksulfid als Weißpigment (Lithopone) hat es stark an Bedeutung verloren. Durch den Zusatz von Blanc fixe werden Kunstdruckpapiere und Photopapiere (Barytpapiere) außerordentlich gut glättbar. In Kunststoffen wird Blanc fixe zur Verbesserung der Verarbeitbarkeit und als "Spacer" (siehe oben) für Weißpigmente und Buntpigmente verwendet. Weitere Anwendungen sind die Erhöhung der Oberflächenhärte und Kratzfestigkeit bei Polyolefinen, die Produktion weißer Filme ohne Farbstich oder transluzierender Kunststoffe und die Verbesserung der Verarbeitbarkeit bei vielen teilkristallinen Thermoplasten. Seine Fähigkeit, Röntgenstrahlung zu absorbieren, wird für medizinische Geräte wie Katheder oder Drainageröhrchen und bei Spielzeug, das von Kindern verschluckt werden kann, ausgenutzt.
Im Synthesefaser-Bereich werden spezifisch strukturierte Faseroberflächen mit einem verbesserten Reibverhalten erhalten. Bei der Papierherstellung geht die Bedeutung von Blanc fixe als Füllstoff infolge einer verbesserten Feinstmahltechnik und der höheren Reinheit von natürlichem Bariumsulfat heute beständig zurück.
Optische Instrumente und Komponenten wie Ulbrichtkugeln, Reflektorpanele oder Pumpkammern, für die ein hoher Reflexionsgrad wichtig ist, werden üblicherweise mit Bariumsulfat beschichtet.
Baryt (Schwerspat) ist heute das einzige technisch genutzte Ausgangsmaterial für die Herstellung von Barium-Metall und aller Barium-Verbindungen.
Bariumsulfat ist als nanometergroßes Pulver nicht selbstentzündlich. Auch als fein verteilte Mischung mit Luft (Staub) unter Einwirkung einer Zündquelle ist Bariumsulfat nicht entzündlich, also besteht keine Möglichkeit einer Staubexplosion.
Vorkommen und Herstellung

Sandrose © Bjorn Wylezich / fotolia.com
In der Natur kommt Bariumsulfat in Form von Kristallen vor, die man ihrer hohen Dichte wegen als Schwerspat (Baryt) bezeichnet. Die säuligen, dünntafeligen oder körnigen Kristalle sind von weißer oder gelblicher Farbe und relativ leicht spaltbar. Durch Verwachsungen der Kristalle kommt es zur Bildung sogenannter Baryt-Rosen. Eine seltene Erscheinungsform im Sand wird Wüstenrose genannt. Die wichtigsten Schwerspat-Lager in Deutschland sind bei Meggen in Westfalen. Wesentlich größere Vorkommen gibt es in China, wo auch die weltweit größten Mengen an Bariumsulfat abgebaut werden. Natürliche Bariumsulfat wird zur Weiterverarbeitung aufgemahlen, wobei im Allgemeinen eine breite Partikelgrößenverteilung entsteht, die bis in den Bereich von 100 nm hinabreichen kann. Die breite Verteilung sichert eine hohe Schüttdichte. Für Anwendungen, bei denen es auf eine sehr reine weiße Farbe oder eine definierte Teilchengrößenverteilung ankommt, wird Bariumsulfat als sogenanntes Blanc fixe (Permanentweiß) durch Fällung hergestellt.
NanoCare - Datenblatt
Weiterführende Informationen
- Kittel, H (1998).Lehrbuch der Lacke und Beschichtungen. 2. Auflage, Hirzel-Verlag, ISBN3777608858.
- Gaechter, R & Mueller, H (1990). Taschenbuch der Kunststoffadditive. 3. Ausgabe, Hanser Fachbuchverlag, ISBN 3446156275.
Nur die Gabe sehr hoher Dosen an Bariumsulfat beeinflusst die Lebensfähigkeit negativ. Weder in Laborversuchen mit Zellen noch in Tierversuchen zeigt es schädigende Effekte.
Untersuchungen am lebenden Organismus - in vivo
Inhalationsexperimente mit Ratten zeigten, dass Bariumsulfat sich nicht in der Lunge ablagert, sondern wieder komplett aus der Lunge der Tiere entfernt wird, die Atemwege werden wieder frei. In medizinischen Fachkreisen nennt man diesen Vorgang Clearance. Schleim, Bakterien und Fremdkörper werden aus dem Körper, in diesem Fall dem Atemtrakt, entfernt, um die Atemwege freizuhalten und Infektionen zu verhindern .
Im Projekt NanoCare wurden sowohl intratracheale Instillationsversuche als auch Inhalationsexperimente mit Ratten durchgeführt. Bei der Instillation wird den Tieren eine Partikel-Suspension in den Rachenraum verabreicht, bei der Inhalation atmen die Tiere über einen bestimmten Zeitraum die Partikel gezielt über die Nase ein. Anschließend werden die verschiedenen Organe der Tiere untersucht. In beiden Versuchsansätzen zeigten die Partikel aus Bariumsulfat keine biologischen Effekte .
Untersuchungen außerhalb des Organismus - in vitro
In vitro Experimente im Projekt NanoCare mit menschlichen Lungenzellen haben gezeigt, dass erst ab einer sehr hohen Dosis von 50µg Partikeln pro cm2 Zellrasen diese Zellen unter Stress stehen und dass dann deren Vitalität abnimmt. Diese Dosis liegt nicht nur weit über einer natürlichen Exposition sondern auch über derjenigen, die durch sachgemäßen Gebrauch des Bariumsulfats entsteht. Bei Untersuchungen mit zehn verschiedenen Zelllinien unterschiedlicher Herkunft mit bis zu 10µg Partikeln pro cm2 Zellrasen zeigten nur embryonale Bindegewebszellen aus Mäusen eine verminderte Zellvitalität und Stress. In allen anderen Zelllinien verursachte BaSO4 keine zellschädigenden Effekte .
Ergänzend zu einfachen Kultursystemen mit nur einer Zelllinie wurden im Projekt NanoCare auch komplexe sog. Kokultursysteme verwendet. Mit Hilfe solcher Systeme kann die in vivo Situation im Körper besser dargestellt werden, weil das Zusammenspiel der Zellen simuliert wird. Bariumsulfat-Partikel lösten in diesen Systemen keine biologischen Effekte aus, die Zellen blieben vital.
Mit Hilfe des sogenannten Vektor-Models, das einige der elementaren Zellfunktionen abbildet , konnten Partner des NanoCare-Projektes zeigen, dass von allen getesteten Materialien BaSO4 die geringsten Auswirkungen zeigt. Eine Konzentration von mehr als 120µg Partikeln pro 106 Fresszellen (damit sind die Zellen vollkommen überladen) führte zu einer Schädigung der Zellen, wobei auch bei dieser ultrahohen Dosis keine Reaktiven Sauerstoffspezies (ROS) in den Zellen detektiert wurden.
Zu einer Umweltexposition mit Bariumsulfat-Nanopartikeln sind derzeit keine Daten vorhanden.
Eingeatmetes Bariumsulfat lagert sich nicht in der Lunge ab und verursacht keine biologischen Effekte. Wenn es über den Magendarm-Trakt aufgenommen wird, wird es unverändert wieder ausgeschieden. Zur Aufnahme über die Haut gibt es keine wissenschaftlichen Studien.
Aufnahme über die Lunge - Inhalation
Die Experimente zeigten, dass durch Einatmen aufgenommenes BaSO4 durch die Selbstreinigung der Lunge (Clearance, Ausscheidungsleistung des Körpers) wieder entfernt wird . Langzeitstudien gibt es derzeit noch nicht.
Aufnahme über den Magen-Darm-Trakt
In der Medizin dient Bariumsulfat in der Zahnheilkunde als Haftgel und aufgrund seiner Undurchlässigkeit für Röntgenstrahlung als Kontrastmittel mit hoher Röntgenstrahlabsorption. Bariumsulfat wird dabei meist in Form von schwer löslichen Suspensionen verwendet. Die Partikel werden nicht resorbiert und eignen sich zur Darstellung des Verdauungstrakts. Das Kontrastmittel wird unverändert als weißer Stuhl wieder ausgeschieden.
Hinsichtlich der Aufnahme und des Risikos für Umweltorganismen von Bariumsulfat-Nanopartikeln sind derzeit keine Daten vorhanden.
Bariumsulfat-Partikel werden im Körper in verschiedene Zelltypen aufgenommen. Der Mechanismus der Aufnahme ist für diese speziellen Partikel noch nicht untersucht.
Verhalten an der Blut-Hirn-Schranke
Nach Einatmen von Bariumsulfat Partikeln erfolgte bereits in der Lunge ein Reinigungsprozess, so dass kein Transport durch den Körper der Tiere stattfand .
Zum Verhalten von Bariumsulfat-Nanopartikeln unter Umweltbedingungen sind derzeit keine Daten vorhanden.
 >
>