Zinkoxid ist ein Alleskönner, wenn es um die technischen Einsatzgebiete geht: zur Gummiherstellung, im Zement und in Farben, aber auch als Katalysator, in medizinischen Produkten und in der Elektronik findet es Verwendung. Zink ist ein essenzielles Element, das der Mensch sowie Tiere und Pflanzen unbedingt zum Leben brauchen.

Hautcreme © Dan Race / Fotolia.com
Wie könnte ich damit in Kontakt kommen?
Der Mensch benötigt täglich zwischen 12 und 15 mg Zink, die er mit der Nahrung aufnimmt. Das Zink liegt dabei meist in der Form von Zinkoxid vor, das sich im Körper auflöst. Wird es zu hoch dosiert, ist auch dieses Material schädlich für den Körper. So können beim Schweißen von Zinkblechen Dämpfe entstehen. Werden sie eingeatmet, können sie die Lunge schädigen. Zinkoxid wird als Nanomaterial auch in Kosmetika als UV-Filter verwendet. Dabei kann gelöstes Zink durchaus über die Haut aufgenommen werden. Da die Haut aber relativ viel Zink für ihren Stoffwechsel benötigt, ist dieser Aufnahmeweg nicht schädlich. Das meiste Zinkoxid nehmen wir aus natürlichen Quellen über die Nahrung auf.
Wie gefährlich ist das Material für Mensch und Umwelt?
In erster Linie hat Zink auch in seiner Form als nanopartikuläres Zinkoxid eine positive Wirkung im Körper, da Zink dort an der Steuerung vieler wichtiger biologischer Prozesse beteiligt ist. Daher wird es auch Zinksalben und anderen medizinischen Produkten beigemischt. In hohen Dosierungen oder am falschen Ort (z.B. als Nanopartikel in der Lunge) kann es aber auch eine giftige Wirkung haben und zum Absterben von Zellen führen (Zinkfieber).
Fazit
Der Mensch kommt im Alltag häufig mit Zinkoxid in Kontakt: von der Nahrung, über Kosmetika bis hin zu technischen Produkten. Da Zink ein essenzielles Element darstellt und sich sein Oxid im Körper auflöst, ist es nur in sehr hohen Dosierungen schädlich für den Menschen.
Nebenbei
- Zink (als Oxid) ist das fünfthäufigste Metall in der Erdkruste
- Als Zinkacetat (E 650) wird Zink auch Lebensmitteln zugesetzt, u.a. um einem Zinkmangel vorzubeugen
Eigenschaften und Anwendungen
Zinkoxid (ZnO) bildet farblose, hexagonale Kristalle oder ein weißes lockeres Pulver. Beim Erhitzen färbt es sich zitronengelb, beim Abkühlen wird es wieder weiß. Es besitzt eine Dichte von 5,61 g/cm³. Ab 1300 °C verdampft es und es sublimiert ab 1800 °C, d. h. es bildet sich keine (flüssige) Schmelze, sondern es geht direkt von dem festen in den gasförmigen Aggregatzustand über.
Zinkoxid hat ein sehr breites, vielfältiges Anwendungsspektrum von der Technik über die Kosmetik bis hin zur Pharmazie. Die Gummi-Industrie ist derzeit das umsatzstärkste Einsatzgebiet von Zinkoxid. Es fördert als Additiv den Vulkanisierungsprozess in der Gummiherstellung von Autoreifen und erhöht besonders durch eine gute Wärmeleitfähigkeit die Abfuhr der durch die Walkarbeit entstehenden Wärme. Zudem erhöht Zinkoxid als Zugabe zu Zement dessen Beständigkeit gegen Wasser und verlängert die Verarbeitungszeit. Auch als Porenfüller in Spachtelmassen oder als graue oder weiße Wand- bzw. Künstlerfarbe werden Zinkstaub und "Zinkweiß" eingesetzt.
Weiterhin dient es als Katalysator in der chemischen Industrie oder zur Herstellung von kosmetischen Erzeugnissen. In der Pharmaindustrie dient es zur Herstellung von Zinksalben, -pasten, -pflastern und –verbänden für die Haut- und Wundbehandlung. Zinkoxid setzt sich mit Wund-sekreten zu antiseptischen und adstringierenden Zinksalzen um.
Verschiedene elektronische Bauelemente wie piezoelektrische Wandler, transparente leitende Oxide, Sensoren, Leuchtdioden oder Optoelektronik- und Spintronik-Bauelemente sind ohne die Verwendung von Zinkoxid derzeit kaum vorstellbar. Als Halbleiter findet Zinkoxid ebenfalls Verwendung als durchsichtige leitende Schicht bei der Herstellung blauer Leuchtdioden (LED), von Flüssigkristallbildschirmen (TFT), Varistoren (VDR) und Dünnschicht-Solarzellen .
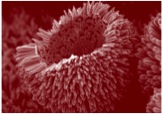
REM Aufnahme eines nanoskaligen Zinkoxid Igels © Empa
Nanopartikuläres Zinkoxid ist im sichtbaren Bereich des Lichtspektrums transparent und wirkt als Filter gegen UV-Strahlung, insbesondere gegen UV-A Strahlen. Die UV-Strahlen werden dabei absorbiert und wie von kleinen Spiegeln reflektiert. Das macht dessen Einsatz als UV-Filter in Sonnenschutzmitteln interessant. Sie sind auch für die empfindliche Haut von Kindern und Allergikern geeignet.
Die Größe der Zinkoxid-Partikel, die für Sonnenschutzmittel verwendet werden, liegt zwischen 20 und 60 nm. Die sehr kleinen ZnO-Nanopartikel werden jedoch vor der Zugabe zu den Sonnenschutzmitteln zusätzlich mit Silizium- oder Aluminiumoxid beschichtet. Sie ballen sich anschließend zu Verbünden von 200-500 nm zusammen. Untersuchungen der Industrie als auch unabhängige Studien, die im Rahmen des EU-Projektes NanoDerm durchgeführt wurden, zeigten, dass diese Partikel aus Sonnenschutzprodukten nicht durch die gesunde Haut in den Körper gelangen und somit keine gesundheitlichen Risiken für den Verbraucher bestehen.
Da Zinkoxid-Nanopartikel sowohl UV-A/UV-B-Schutz und Transparenz aufweisen und wie oben beschrieben eine antibakterielle und fungistatische Wirkung besitzen, wird es auch in Textilien, in Klarlacken im Holz- und Möbelbereich und darüber hinaus in transparenten Kunststoffen und Kunststofffilmen (Kunststoffgläser) eingesetzt. Diese zeichnen sich durch eine hohe Transparenz (>90%Transmission) im sichtbaren Spektralbereich und durch eine UV-Undurchlässigkeit (<10%Transmission) für Wellenlängen unterhalb von 360 nm aus.
Zinkoxid ist als nanometergroßes Pulver nicht selbstentzündlich. Auch als fein verteilte Mischung mit Luft (Staub) unter Einwirkung einer Zündquelle ist Zinkoxid nicht entzündlich, also besteht keine Möglichkeit einer Staubexplosion.
Vorkommen und Herstellung
Zinkoxid (ZnO) kommt in der Natur als grobkörniges Mineral (Zinkit) vor. Technisch wird es durch die Oxidation von Zink bzw. Zinkdampf mit Luftsauerstoff (Zinkweiß) oder durch Glühen (Calcination) verschiedener Vorstoffe wie Zinkhydroxid, Zinkcarbonat oder Zinknitrat gewonnen. Technische Zinkoxide sind häufig bleihaltig und müssen dann mit dem entsprechenden Gefahrensymbol (Xn) gekennzeichnet werden.
NanoCare - Datenblatt
Weiterführende Informationen
- Roempp-online.de (DE): Zinkoxid (Stand letzter Zugang: Jul 2011).
- EU-Projekt NanoDerm (Stand letzter Zugang: Jul 2017).
- BASF Infoservice (DE): Die neue Generation von UV-Filtern: zuverlässiger Allroundschutz für den ganzen Tag, Wissenschaft populär.
- BfR Stellungnahme Nr. 037/2010 (18.06.2010). Sonnenschutzmittel: Zinkoxid als UV-Filter ist nach derzeitigem Kenntnisstand gesundheitlich unbedenklich (PDF) .
Zinkoxid kommt in Sonnencreme, Textilien, Lacken oder auch Kunststoffen vor. In hohen Dosierungen kann es eine giftige Wirkung haben.
Allgemeine Gefährdung
Es ist bekannt, dass die Inhalation von Zinkoxid-Dämpfen bei Schweissarbeiten zu dem sogenannten Metallrauchfieber führen kann . Es handelt sich um eine grippeähnliche Krankheit, die sich nach einigen Tagen wieder zurückbildet, jedoch unter fortgesetzter Exposition zu Einschränkungen der Lungenfunktion führen kann. Viel wahrscheinlicher als die Inhalation ist jedoch eine Aufnahme dieser Nanopartikel über die Haut, da nanopartikuläres ZnO als anorganischer (mineralischer) UV-Filter in Sonnencremes und Kosmetika verwendet wird.
Untersuchungen am lebenden Organismus - in vivo
Die Verabreichung von feinen oder nanoskaligen Zinkoxid Partikeln in die Lunge von Mäusen oder Ratten verursacht eine starke, jedoch vorübergehende Lungenentzündung . Interessanterweise war sowohl die Stärke als auch der Verlauf dieser Reaktion praktisch identisch für feines oder nanoskaliges ZnO.
Untersuchung außerhalb des Körpers – in vitro
Die meisten in vitro Studien zeigen eine relativ hohe Toxizität von Zinkoxid (ZnO) -Nanopartikel für Zellen von verschiedenen Geweben als auch von unterschiedlichen Organismen. Dabei zeigen Zinkoxid Partikel eine sehr steile Dosis-Wirkungs-Kurve, d.h. die toxische Wirkung steigt ab einer gewissen Konzentration sehr rasch an. Für die meisten Zelltypen liegt dieser Wert im Bereich von 10-20 µg/ml.
Im Projekt NanoCare durchgeführte Studien mit elf verschiedenen Zelllinien unterschiedlicher Herkunft zeigten, dass die Zelllinien unterschiedlich sensibel auf Zinkoxid Partikel reagieren. Auch hier wurde bei einigen Zelllinien eine relativ hohe Toxizität schon bei geringen Konzentrationen festgestellt (LOEL ab 5µg/cm2 oder ca. 16µg/ml). Die Schwellenwerte für in vitro Tests auf Apoptose lagen bei einigen Zellen bei 7,5-10µg/cm2 .
Ergänzend zu einfachen Kultursystemen mit nur einer Zelllinie wurden im Projekt NanoCare auch komplexe Kokultursysteme verwendet. Mit Hilfe solcher Systeme kann die in vivo Situation im Körper besser dargestellt werden, weil das Zusammenspiel der Zellen simuliert wird. Zinkoxid Partikel verursachten in diesen Systemen die verstärkte Bildung von Entzündungsmarkern .
Der Mechanismus, der für die hohe Toxizität von Zinkoxid Partikeln verantwortlich ist, ist noch nicht vollständig geklärt. Es scheint aber, dass freigesetzte Zink-Ionen und reaktive Sauerstoffradikale eine wichtige Rolle spielen . Auch der Einfluss der Form und der Größe der Zinkoxid Partikel auf die toxische Wirkung ist noch unklar. Mehrere Arbeiten konnten jedoch keine größenabhängigen Effekte nachweisen . Durch die Beschichtung von Zinkoxid Nanopartikeln mit Gold oder Aluminium konnte deren Toxizität stark gesenkt werden . Es wurde darum postuliert, dass wohl eher die elektronischen Eigenschaften oder die Löslichkeit als die Größe der Partikel wichtig für ihre zellulären Effekte sind.
Die Möglichkeit, die Toxizität von Zinkoxid Nanopartikel durch gezielte Modifikationen zu verändern, macht diese Nanoteilchen auch für medizinische Anwendungen interessant . Außerdem scheinen Zinkoxid Partikel vor allem für Krebszellen (also auch für viele in Zellkultursystemen verwendete Zelllinien) nicht aber für normale Zellen sehr toxisch zu sein . Zinkoxid Nanopartikel werden daher zur potentiellen Krebsbekämpfung oder als Vehikel für die Verabreichung von Medikamenten erforscht.
Durch den Einsatz von nanoskaligem Zinkoxid (ZnO) in Kosmetika, Beschichtungen und Reinigungsmitteln ist mit einem – im Vergleich zu anderen Nanopartikeln – relativ hohen Eintrag in Gewässer zu rechnen. Zinkoxid Nanopartikel lösen sich in Flüssigkeiten schnell auf. Tatsächlich gemessene Umweltkonzentrationen gibt es für Zinkoxid Nanopartikel noch nicht.

Wasserprobe © Vasily-Merushev/Fotolia.com
Die zu erwartenden Zinkoxid Nanopartikel-Konzentrationen in der Umwelt wurden mittels Computermodellen geschätzt. Im Vergleich zu anderen Nanomaterialien sind die erwarteten Zinkoxid-Konzentrationen sehr hoch. Das ergibt sich aus vielen Anwendungen, wie beispielsweise in Textilen und Sonnenschutzcreme, bei denen das Zink nach Gebrauch direkt in die Umwelt freigesetzt wird. Nur ein geringer Teil der freigesetzten Zinkoxid Nanopartikel gelangt in die Luft. Die Konzentrationen an Zinkoxid Nanopartikeln in Europäischen Gewässern unterliegen in Anhängigkeit von Besiedlungs- und Kläranlagendichte, sowie der Jahreszeiten starken Schwankungen. Geringe Mengen an Zink werden in Boden und Luft erwartet .
Abhängig vom betrachteten Umweltkompartiment ergeben im Zusammenhang mit den für aquatische Organismen bekanntermaßen toxischen Konzentrationen Risikoquotienten von unter 1 bis ~ 10. Dies ist ein Hinweis darauf, dass zumindest für bestimmte Kompartimente (z.B. Abwässer) ein Umweltrisiko durch Zinkoxid-Nanopartikel nicht ausgeschlossen werden kann (z.B. im Boden nach Ausbringung von Klärschlamm). Diese theoretisch ermittelten Werte müssen jedoch zukünftig durch Messwerte experimentell bestätigt werden .
Bei der Herstellung und Verarbeitung von Zinkoxid-Nanopartikeln besteht die Möglichkeit einer Aufnahme durch Einatmen. Aus Sonnenschutzprodukten gelangen keine Partikel durch die gesunde Haut in den Körper, könnten aber durch Verschlucken aufgenommen werden.
Aufnahme über die Lunge - Inhalation
Erste Studien am Tiermodell zeigen, dass die Inhalation von Zinkoxid Nanopartikeln eine relativ starke, aber vorübergehende Entzündung der Lunge bewirken kann . Dies ist ähnlich dem sogenannten Metallrauchfieber, einer grippeähnlichen Krankheit mit Entzündung der Atemwege, welches bei Schweißarbeiten durch Einatmung von Metalldämpfen (vor allem Zinkdämpfe) entstehen kann.
Aufnahme über die Haut - Dermal
Da Zinkoxid Nanopartikel als anorganische (mineralische) UV-Filter in Sonnencremes und Kosmetika eingesetzt werden, ist es wichtig zu wissen, ob diese Partikel über die Haut aufgenommen werden. Die Größe der Zinkoxid Partikel, die für Sonnenschutzmittel verwendet werden, liegt zwischen 20 bis 60 nm. Die sehr kleinen Zinkoxid Nanopartikel werden jedoch vor der Zugabe zu den Sonnenschutzmitteln zusätzlich mit Silizium- oder Aluminiumoxid beschichtet. Sie ballen sich anschließend zu Aggregaten von 200-500 nm zusammen.
Untersuchungen der Industrie als auch unabhängige Studien, die im Rahmen des EU-Projektes NanoDerm durchgeführt wurden, zeigten, dass diese Partikel aus Sonnenschutzprodukten nicht durch die gesunde Haut in den Körper gelangen und somit keine gesundheitlichen Risiken für den Verbraucher bestehen . Bisherige Studien wurden jedoch meistens am Tiermodell oder in Zellkulturen durchgeführt.
Eine neue Studie, in der ZnO-haltige Sonnencreme unter realitätsnahen Bedingungen am Menschen getestet wurde, hat nun jedoch kleine Mengen von diesem markierten Zink im Blut und Urin gemessen . Diese war aber nur 1/1000 der im Blut bereits natürlich vorhandenen Zink-Konzentration. Auch ist noch nicht klar, ob Zink als Zinkoxid Partikel oder als gelöste Zink-Ionen über die Haut aufgenommen wurde.
Infos dazu aus dem Bundesgesetz (Stand 2010):
In der Ausgabe des Bundesgesetzblatts Teil I, Nr. 66 vom 22.12.2010 erschien die 56. Verordnung zur Änderung der Kosmetik-Verordnung . Folgender Inhalt ist hier bemerkenswert.
- Satz 1 wird wie folgt gefasst: "Die Verwendung von beschichtetem mikrofeinem Zinkoxid bis zu einer Höchstmenge von 25% als UV-Filter ist bis zum Ablauf des 31. Dezember 2011 gestattet."
- Nach Satz 1 wird folgender Satz 2 eingefügt: "Eine Verwendung in treibmittel-basierten Sprays ist nicht gestattet."
Aufnahme über den Magen-Darm-Trakt
Eine Studie an Mäusen hat gezeigt, dass nach der oralen Verabreichung von Zinkoxid-Nanopartikeln erhöhte Konzentrationen von Zink in Leber, Herz, Milz, Magen und Knochen gefunden wurde .
Das Element Zink ist für alle Lebewesen in geringen Dosen lebenswichtig, in hohe Dosen jedoch bekanntermaßen toxisch. Diese Beobachtung spiegelt sich in den Ergebnissen zur Toxizität von nanoskaligem Zinkoxid (ZnO) wider. Zinkoxid Nanopartikel lösen sich generell schnell in Flüssigkeiten auf, so dass neben den Partikeln immer auch Ionen vorliegen. Deshalb gibt es für dieses Nanomaterial viele vergleichende Untersuchungen zur Wirkung von Zinksalz, Nanopartikel und Mikropartikeln in verschiedenen Umwelttestorganismen.
Zink und Zinkoxid sind bekanntermaßen antibakteriell wirksam (Einsatz in Zinksalben) und demzufolge wurde eine Hemmung des Wachstums verschiedener Bakterienarten durch Zinkoxid Nanopartikel beobachtet. Es wird angenommen, dass die Toxizität größtenteils von den freigesetzten Ionen ausgeht. Die Wachstumshemmung war unter Lichteinfluss verstärkt, und durch kleinere Partikel stärker als durch größere. Oxidativer Stress und eine Schädigung der äußeren Membran wird als Mechanismus der Toxizität vermutet. Weiterhin schädigen Zinkoxid Nanopartikel in einigen Bakterienarten das Erbgut. Durch die unterschiedliche Empfindlichkeit einzelner Bakterienarten verändert sich die Zusammensetzung von Bakteriengemeinschaften unter dem Einfluss von Zinkoxid Nanopartikeln. Die schädliche Wirkung von Zink in hohen Dosen kann Auswirkungen auf die zahlreichen wichtigen Funktionen haben, die Bakterien in der Umwelt übernehmen, beispielsweise die Stickstoff- und Methanfixierung .
 Die generellen Anzeichen einer Schädigung des Fisch-Organismus durch zu hohe Zink-Konzentrationen reichen von Entwicklungsverzögerungen bis zur Schädigung einzelner Organe oder des Immunsystems. Eine genauere Untersuchung des Wirkmechanismus ergab eine Bildung von reaktivem Sauerstoff durch Zinkoxidpartikel als mögliche Ursache der Toxizität. Einige Fischarten, jedoch nicht alle nehmen Zinkoxid Nanopartikel auf und Zink konnte in zahlreichen Geweben (Leber, Gehirn, Kiemen) nachgewiesen werden. In zahlreiche Fischstudien lösten die Nanopartikel einen stärkeren Effekt aus als Zink-Ionen. In einigen Studien wurde hingegen keinerlei Unterschied ermittelt. In jedem Fall wird den gelösten Ionen wird ein Teil der Wirkung zugeschrieben, welche offensichtlich durch die Partikel verstärkt werden kann .
Die generellen Anzeichen einer Schädigung des Fisch-Organismus durch zu hohe Zink-Konzentrationen reichen von Entwicklungsverzögerungen bis zur Schädigung einzelner Organe oder des Immunsystems. Eine genauere Untersuchung des Wirkmechanismus ergab eine Bildung von reaktivem Sauerstoff durch Zinkoxidpartikel als mögliche Ursache der Toxizität. Einige Fischarten, jedoch nicht alle nehmen Zinkoxid Nanopartikel auf und Zink konnte in zahlreichen Geweben (Leber, Gehirn, Kiemen) nachgewiesen werden. In zahlreiche Fischstudien lösten die Nanopartikel einen stärkeren Effekt aus als Zink-Ionen. In einigen Studien wurde hingegen keinerlei Unterschied ermittelt. In jedem Fall wird den gelösten Ionen wird ein Teil der Wirkung zugeschrieben, welche offensichtlich durch die Partikel verstärkt werden kann .
 Für Wasserflöhe ist Zink ab einer gewissen Konzentration toxisch. Organische Substanzen die natürlich in Gewässern vorkommen, können den toxischen Effekt der Zinkoxid Nanopartikel herabsetzen. Da Wasserflöhe das Wasser zur Nahrungsaufnahme filtrieren, gelangen Nanopartikel direkt in den Körper der Wasserflöhe, die sie aber wieder ausscheiden. In Wasserflöhen lösten Zinkoxid Nanopartikel gleiche toxische Wirkungen wie Ionen aus. Die Partikel waren umso schädlicher, je mehr Ionen sie freisetzten.
Für Wasserflöhe ist Zink ab einer gewissen Konzentration toxisch. Organische Substanzen die natürlich in Gewässern vorkommen, können den toxischen Effekt der Zinkoxid Nanopartikel herabsetzen. Da Wasserflöhe das Wasser zur Nahrungsaufnahme filtrieren, gelangen Nanopartikel direkt in den Körper der Wasserflöhe, die sie aber wieder ausscheiden. In Wasserflöhen lösten Zinkoxid Nanopartikel gleiche toxische Wirkungen wie Ionen aus. Die Partikel waren umso schädlicher, je mehr Ionen sie freisetzten.
Ähnliche Beobachtungen für Zinkoxid Nanopartikel wurden auch in einer Reihe weiterer Krebstiere sowie Plankton gemacht. Die Wirkung von Zinkoxid Nanopartikeln und Zink-Ionen unterschied sich in Kellerasseln nicht .
Der Einfluss von Zinkoxid Nanopartikeln auf Wachstum, Fortpflanzung und Verhalten von Fadenwürmern war mit dem von Zink-Ionen vergleichbar, wobei einige Ergebnisse auch auf eine stärkere Wirkung kleinerer Partikel hindeuten. Auch in Fadenwürmern verursachen die Partikel oxidativen Stress. Licht kann die Toxizität der Zinkoxid Nanopartikel verstärken. In Regenwürmern lösen Zinkoxid Nanopartikel ähnliche Effekte aus wie im Fadenwurm. Jedoch lösen bei diesem Organismus Ionen eine größere Toxizität aus als Nanopartikel .

Zinkoxid Nanopartikel werden von Muscheln und Schnecken aufgenommen und wirken in hohen Konzentrationen toxisch. Auch hier wurde oxidativer Stress als Wirkweise nachgewiesen. Gegenüber Seeigelembryonen wirkt Zink ebenfalls toxisch, hier sind vorrangig die freigesetzten Ionen für die Giftigkeit der Partikel verantwortlich. Eine andere Studie dahingegen zeigt, dass die Nanopartikel toxischer sind als die Ionen. Zudem wurde bewiesen, dass durch die Nanopartikel die Eihülle verändert wird, wodurch andere Kontaminanten in den Embryo gelangen könnten.

Krallenfroschembryonen nehmen Zinkoxid Nanopartikel ebenfalls auf. Die Partikel lösen oxidativen Stress aus, was zu einer Schädigung von Zellen führt .

Zinkoxid Nanopartikel beeinflussen das Nervensystem und senken die Überlebensrate von Bienen. Bei Springschwänzen bewirken Zinkoxid Nanopartikel und Zink-Ionen gleichermaßen Schädigungen im Erbgut und in der Fortpflanzungsfähigkeit. Die Größe der Partikel hat keinen Einfluss auf die toxische Wirkung. Die Tiere meiden mit Zink kontaminierten Boden .
 Für Algen ist Zink ein toxisches Element, die wirksame Komponente ist dabei das Zink-Ion. Sowohl Zinkoxid Nanopartikel als auch gröbere Partikel setzen diese Ionen in verschiedenen Anteilen frei, und sind daher auch für Algen toxisch. Inwieweit die schädliche Wirkung von Form und Größe der Partikel abhängt, wird unterschiedlich bewertet. Einige Studien finden keine Abhängigkeit, während andere eine gewisse Abhängigkeit sowohl von der Form, als auch der Größe der Partikel sehen. Zink löst in Algen eine verminderte Wachstumsrate und oxidativen Stress aus. Zinkoxid Nanopartikel werden in Algenzellen aufgenommen .
Für Algen ist Zink ein toxisches Element, die wirksame Komponente ist dabei das Zink-Ion. Sowohl Zinkoxid Nanopartikel als auch gröbere Partikel setzen diese Ionen in verschiedenen Anteilen frei, und sind daher auch für Algen toxisch. Inwieweit die schädliche Wirkung von Form und Größe der Partikel abhängt, wird unterschiedlich bewertet. Einige Studien finden keine Abhängigkeit, während andere eine gewisse Abhängigkeit sowohl von der Form, als auch der Größe der Partikel sehen. Zink löst in Algen eine verminderte Wachstumsrate und oxidativen Stress aus. Zinkoxid Nanopartikel werden in Algenzellen aufgenommen .

Zink kann auch für Pflanzen toxisch sein, wobei die einzelnen Arten unterschiedlich empfindlich sind. Überwiegend werden die aus den Nanopartikeln freigesetzten Ionen für die Pflanzentoxizität verantwortlich gemacht. In erster Linie sind die Wurzeln der Pflanzen in ihrem Wachstum beeinträchtigt, denn diese haben den ersten Kontakt mit den Zinkoxid Nanopartikeln. Für die Samen wurde eine verzögerte Keimung beobachtet. Zink wird in die Pflanzen aufgenommen und verteilt sich mehr oder weniger in Wurzeln, Spross, Blättern und Früchten. Auch in Pflanzen bewirken Zinkoxid Nanopartikel die Entstehung von oxidativem Stress .
Viele Arbeiten, jedoch nicht alle, führen die schädliche Wirkung des Zinks auf die Freisetzung von Ionen aus den Nanopartikeln zurück. Insgesamt lösen Partikel verschiedener Größen und Zink-Ionen ähnliche Symptome aus, beispielsweise oxidativen Stress, welcher in fast allen untersuchten Organismengruppen nachgewiesen wurde. Die Wirkstärke kann sich jedoch unterscheiden.
Weiterführende Literatur
- Weitere evaluierte Veröffentlichungen zu diesem Nanomaterial finden Sie hier (PDF; 85 KB )
Im wässrigen Milieu des menschlichen Organismus lösen sich Zinkoxid Nanopartikel teilweise oder ganz auf und es werden Zink-Ionen freigesetzt.
Aufnahmeverhalten in Zellen
Der Auflösungsprozess ist jedoch für unterschiedliche Zinkoxid Partikel nicht immer gleich effizient und ist außerdem abhängig von der genauen Zusammensetzung der wässrigen Lösung. Ob Zellen nun Zinkoxid Partikel oder gelöste Zink-Ionen aufnehmen scheint also von der Stabilität der Nanopartikel in der jeweiligen Umgebung abhängig zu sein. In der Literatur findet man folglich Studien, welche eine Aufnahme von Zinkoxid Partikeln in der Zelle beschreiben als auch solche, die keine Partikel beobachten . Falls partikuläres Zinkoxid aufgenommen wird, könnte deren Auflösung in der Zelle zu lokal sehr hohen Konzentration von Zink-Ionen und somit zu Nanopartikel-spezifischen Reaktionen führen.
Zinkoxid Nanopartikel sind positiv geladen und gehören zu den löslichen Nanopartikeln. Sie zeigen eine hohe Agglomerationsneigung und neigen zur Auflösung, d.h. neben den eigentlichen Partikeln befinden sich in einer wässrigen Lösung auch immer gelöste Zink-Ionen. Die meisten Erkenntnisse zum Verhalten von Zinkoxid Nanopartikeln sind für Boden und Wasser verfügbar, während für das Verhalten in Luft wenig Information vorliegt.
In normalem Leitungswasser sind Zinkoxid Nanopartikel wenig stabil und sedimentieren. Bei einem Zusatz von Huminsäure, eine in natürlichen Gewässern vorkommende Substanz, werden die Partikel hingegen stabilisiert und damit ihre Mobilität erhöht. Die Löslichkeit der Nanopartikel hängt von Partikeleigenschaften wie der Größe, aber auch von der Art und Zusammensetzung des umgebenden Milieus ab. Unter Bedingungen, wie sie in einer Kläranlage vorherrschen wird eine vollständige Auflösung der Partikel angenommen. Faktoren wie Umgebungstemperatur und pH-Wert beeinflussen die Agglomeration und die Ionenfreisetzung. Auf die Art der Oberflächenbeschichtungen kann das Löslichkeitsverhalten von Zinkoxidnanopartikeln beeinflussen .
Zinkoxid Nanopartikel die in Sedimente oder Böden gelangen, werden als wenig mobil eingeschätzt, das bedeutet, sie verbleiben mehr oder weniger am Ort ihres Eintrages in die Umwelt. Phosphate, wie sie im Grundwasser enthalten sind, erleichtern hingegen den Transport von Zinkoxid Nanopartikeln .
Zinkoxid Nanopartikel sind photokatalytisch aktiv und können zum Abbau von chemischen Substanzen in der Umwelt genutzt werden .
Zinkoxid Nanopartikel gelten unter Umweltbedingungen als wenig stabil, da sie einer Tendenz zur Auflösung unterliegen. Die Geschwindigkeit des Prozesses wird durch die jeweils vorherrschenden Umweltbedingungen beeinflusst. Aufgrund ihrer Sedimentationsneigung lagert sich ein Großteil der in die Umwelt freigesetzten Zinkoxid Nanopartikel in Sedimenten ab.
 >
>