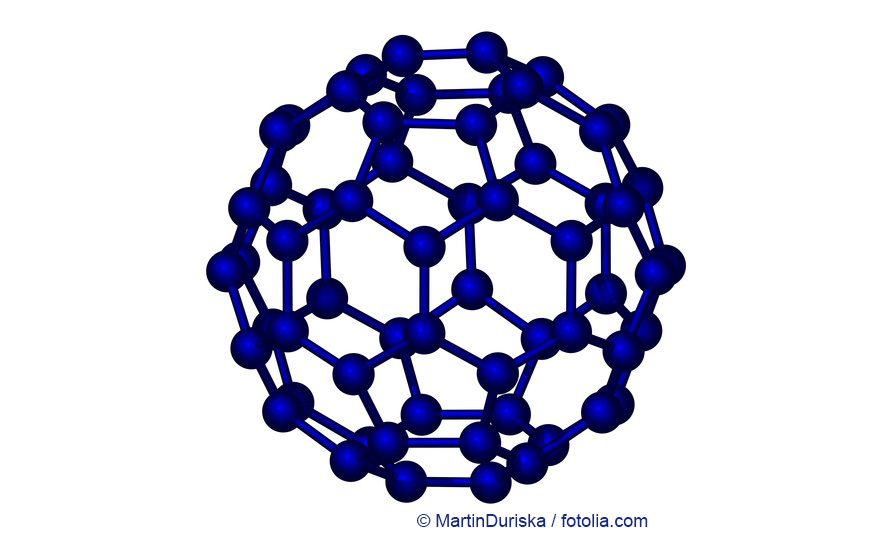
Buckminsterfulleren © Martin Duriska / fotolia.com
Fullerene, die auch Buckminsterfullerene oder Bucky Balls genannt werden, bestehen ausschließlich aus Kohlenstoff. Das einfachste, C60 genannt, ist wie ein Fußball aufgebaut: aus 20 Sechs- und 12 Fünfecken, wobei die Ecken jeweils von einem Kohlenstoffatom besetzt sind. Noch gibt es nur sehr wenige Anwendungen für diese Materialklasse.
Wie könnte ich damit in Kontakt kommen?
Zwei prominente Anwendungen existieren bereits, jedoch nicht im europäischen Raum. Zum einen werden einige Kunststoffe mit Fullerenen verbessert, zum anderen gibt es eine japanische Firma, die Kosmetika mit Fullerenen herstellt. Da Fullerene die Eigenschaft haben, besonders aggressive Sauerstoffmoleküle abzufangen (Radikalfänger), werden sie relativ teuren Anti-Ageing-Cremes zugesetzt. Auf diesem Weg geraten sie natürlich in direkten Kontakt mit der Haut. Weitere mögliche Anwendungen wurden bisher noch nicht in die Praxis umgesetzt.
Wie gefährlich ist das Material für Mensch und Umwelt?
Bisher gibt es nur wenige verlässliche Studien zu ihrer gesundheitlichen Wirkung auf Mensch oder Tier. Die Verteilung im Körper wurde in einigen Studien untersucht und es konnte nachgewiesen werden, dass diese doch sehr kleinen Partikel (nur 0,7 nm im Durchmesser) Gewebeschranken durchdringen können. Hinweise auf Veränderungen im Gewebe und mögliche nachfolgende Erkrankungen gibt es jedoch bisher keine. Dies passiert allerdings nur, wenn einzelne Fullerene auftreten, normalerweise sind sie aber verklumpt (agglomeriert) und dadurch wird das Durchdringen der Gewebebarrieren erheblich reduziert.
Fazit
Die produzierte Menge und vor allem die in Produkten tatsächlich eingesetzte Menge ist aktuell weltweit so gering, dass keine negativen Wirkungen davon ausgehen können. Das kann sich ändern, sollten weitere Produkte auf den Markt kommen, zu denen die Fullerene in erheblichen Mengen beigesetzt werden.
Eigenschaften und Anwendungen
Fullerene sind kugelförmige Moleküle aus Kohlenstoffatomen. Das sogenannte Buckminsterfulleren C60 (engl.Bucky Ball) ist das derzeit am Besten erforschte Molekül dieser Art. Ihren Namen erhielten diese faszinierenden Moleküle nach dem Architekten Richard Buckminster Fuller (1895-1983). Für die Expo 1967 in Montreal entwarf er eine Kuppelkonstruktion aus sechseckigen und fünfeckigen Zellen (geodätische Kuppel). Diese geodätischen Kuppeln ähneln den Fullerenen stark in ihrer Architektur.

Das C60-Molekül beispielsweise hat einen Durchmesser von 0,7 nm und ist genau wie ein Fußball aus 20 Sechsringen und 12 Fünfringen aufgebaut, weshalb man oft auch vom Fußballmolekül spricht. Der Größenvergleich ergibt, dass sich ein Fulleren im Verhältnis zu einem Fußball so verhält wie der Fußball zur Erde. Fullerene sind ebenso wie Diamant oder Graphit eine Kohlenstoffmodifikation. Die Hohlkugelgestalt der Fullerene führt zu einer im Vergleich zu Graphit (2,1-2,3 g/cm³) oder gar Diamant (3,51 g/cm³) sehr geringen Dichte (1,68 g/cm³). Im Gegensatz zu Graphit sind die Fullerene nicht elektrisch leitend.
Das C60 bildet gelbe Kristalle, beim Lösen in organischen Lösungsmitteln (bspw. Toluol) bildet es jedoch eine markant weinrote Farbe aus. Damit sind sie als einzige allotrope Modifikation des Kohlenstoffs in organischen Lösungsmitteln löslich. Durch UV-Strahlung, besonders in Gegenwart von O2, wird der Fullerenkäfig zerstört.
Die C60-Fullerene sind die kleinsten Fullerene einer großen Anzahl allotroper Fullerene. Das nächstgrößere Fulleren (C70) bspw. hat die Struktur eines Rugbyballs. Auch andere Cn-Moleküle wurden bislang isoliert (n = 74, 76, 78, 80, 84, 90, 94). Es werden zudem C240 und C540-Moleküle vermutet.
Anwendung finden die Fullerene derzeit im Kosmetik- sowie dem Sportartikelbereich. In Anti-Aging-Cremes findet das C60-Molekül bspw. Einsatz aufgrund seiner hohen Elektronenaffinität (Radikalfänger), dadurch soll es viele freie Radikale (reaktive molekulare Spezies), die für den Alterungsprozess der Haut verantwortlich sind, aufnehmen können. Bei der Sportgeräteherstellung finden die Fullerene vor allem ihren Einsatz beim Bau von Tennis-, Badminton- oder Golfschlägern. Hier werden C60-Moleküle in Schaft und Rahmen verbaut um so sehr dünnwandige und somit leichte aber auch stabilere Carbon-Konstruktionen zu ermöglichen.
Da Fullerene nicht biologisch abbaubar sind und die Datenlage zur Toxizität noch sehr gering ist, verzichten Firmen wie Ciba (seit 01.04.2009 Teil der BASF SE) und Novartis derzeit auf ihren Einsatz.
Fullerene sind nicht selbstentzündlich. Als fein verteilte Mischung mit Luft (Staub) unter Einwirkung einer Zündquelle sind Fullerene entzündlich (Staubexplosion). Das Verhalten bei einer Staubexplosion ist vergleichbar mit dem anderer, kohlenstoffbasierter Materialien.
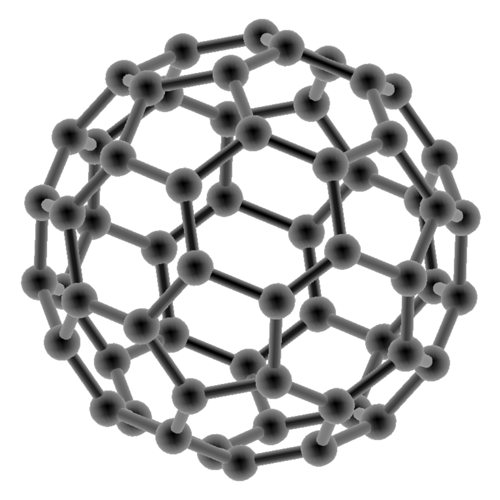
Buckminsterfulleren © www.biocrawler.com
Vorkommen und Herstellung
Fullerene kommen in der Natur in verschiedenen Gesteinen vor. Man geht davon aus, dass Fullerene bereits frühzeitig unbeabsichtigt von Menschen synthetisiert wurden und als Ruß auf Höhlenwänden abgelagert wurden. Die Möglichkeit der Existenz von Fullerenen wurde 1970 von dem japanischen Chemiker Eiji Osawa auf Grundlage von Berechnungen vorhergesagt. Davidson und Haymet bestätigten im Jahre 1981 und 1985 die Rechnungen von Osawa. Im Jahre 1985 gaben Curl, Kroto und Smalley erstmals die Herstellung eines Fullerens, nämlich C60, in sehr geringen Mengen mittels Verdampfung von Graphit im Laserstrahl bekannt . Im Jahre 1996 wurden sie hierfür mit dem Nobelpreis für Chemie ausgezeichnet . Die Synthese von Buckminsterfullerenen in größeren Mengen gelang im Jahre 1990 durch Krätschmer und Huffmann . Ihr Prozess beruht auf dem Verdampfen von Graphit im Lichtbogen oder mit Hilfe des elektrischen Stroms in einer Unterdruckatmosphäre aus Helium oder Argon.
Es gibt erst wenige Anwendungen für diese Materialklasse, so dass die Exposition von Menschen mit nanogroßen Fullerenen sehr gering ausfällt.
Allgemeine Gefährdung
Unbeabsichtigt können Fullerene in sehr geringen Mengen bei Verbrennungsprozessen entstehen und so in die Luft gelangen. Noch gibt es kaum Anwendungen für diese Materialklasse, so dass die Exposition von Mensch und Umwelt mit nanogroßen Fullerenen sehr gering ausfällt. Deshalb sind epidemiologische Daten zu Fullerenen auch bis heute nicht vorhanden.
Untersuchungen am lebenden Organismus - in vivo
Unabhängig von der Verabreichung der nicht-oberflächenmodifizierten Fullerene über die Lunge (Inhalation, Instillation) verursachen diese dort nur eine vorübergehende Entzündungsreaktion. Auch oral zugeführte Fullerene in niedriger Dosis konnten in Ratten eine ähnliche vorübergehende Entzündungsreaktion in der Leber und Lunge, aber nicht im Magen-Darm-Trakt, auslösen .
Dank der Vorbehandlung mit Fullerenen konnte eine Vergiftungsreaktion in der Leber der Versuchstiere mit Tetrachlorkohlenstoff verhindert werden, was auf die Fähigkeit der Fullerene, freie Radikale zu binden, zurückzuführen ist .
Über eine Funktionalisierung der Fulleren-Oberfläche z.B. mit mit Hydroxylgruppen oder anderen funktionellen Gruppen, kann die Löslichkeit und darüber das toxische Verhalten der Nanomaterialien drastisch verändert werden. Je nach Oberflächenmodifikation, Aufbereitung der Nanomaterial Suspensionen oder der Verabreichungsart der Fullerene ergeben sich unterschiedliche Ergebnisse in Bezug auf deren Toxizität, die nicht immer miteinander vergleichbar sind.
Untersuchung außerhalb des Körpers – in vitro

Fulleren mit Kolben © madamlead / Fotolia.com
Fullerene sind aufgrund ihrer chemischen Eigenschaften nur schwer in Wasser suspendierbar. Sie verklumpen zu stabilen Aggregaten mit einem Durchmesser von bis zu 500 nm, sind aber dennoch klein genug, um von Lungenzellen aufgenommen zu werden. Oberflächen-modifizierte Fullerene werden im Folgenden nicht berücksichtigt.
Die Toxizität der Fullerene wird sehr kontrovers diskutiert, was auf die Aufbereitung der Nanopartikel-Suspension für die späteren in vitro Untersuchungen an Zellkulturen zurückzuführen ist. Werden die Fullerene zunächst mit Hilfe eines Lösungsmittels wie Tetrahydrofuran suspendiert und anschließend in Wasser überführt, entstehen bei diesem Prozess ungewollte Nebenprodukte wie z.B. Tetrahydrofuran Peroxide. Insbesondere diese Nebenprodukte sind für die meisten akut toxischen Effekte verantwortlich, da nach einem Entfernen durch zusätzliche Waschschritte keine akut toxischen Effekte mehr gemessen werden können. Diese Tatsache wurde in mehreren Studien bestätigt .
Reine Fullerene, die ohne zusätzliche Lösungsmittel bzw. Nebenprodukte in Zellkulturversuchen getestet wurden, verursachten keine Reaktion in Lungen- und/oder Hautzellen.
Fullerene bestehen ausschließlich aus Kohlenstoff, der in allen Lebewesen und der Luft häufig vorkommt. Daher ist ein spezifischer Nachweis dieser Nanomaterialien in der Umwelt sehr schwierig und derzeit sind nur wenige Angaben zu den in der Umwelt anzutreffenden Mengen an Fullerenen verfügbar.

Rauchender Schornstein © spuno / fotolia.com
Als Quellen für Fullerene kommen neben den Produktionsstätten auch Verbrennungsrückstände (Ruß) aus Kerzen, Motoren, Flugzeug-Turbinen sowie dem Umgang mit diesen Nanomaterialien im Labor in Frage . Fullerene können auch auf natürlichem Wege durch Blitz- oder Meteoriteneinschläge entstehen. Sie werden zunächst in die Luft freigesetzt und dann über den Regen in Böden oder Oberflächengewässer transportiert. Fullerole, das sind mit Hydroxyl-Gruppen besetzte Fullerene, können aufgrund ihrer veränderten Oberfläche durch bestimmte Pilze abgebaut werden, bei Fullerenen ist das nicht möglich .
Wenige Studien beschreiben den Nachweis von Fullerenen in Umweltproben. Spuren von Fulleren Nanomaterialien wurden in Aerosolen des Mittelmeeres, in Sand aus Saudi-Arabien, in Flusssediment aus Spanien, in Wässern und Sedimenten aus Barcelona und Brasilien, sowie in einigen Oberflächengewässern aus Taiwan gefunden . Diese geringen Mengen von Fulleren Nanomaterialien stellen jedoch keine Gefahr für die jeweiligen Umweltorganismen dar (vgl. Aufnahme & Risiko für Umweltorganismen).
Allerdings konnte in industriell genutzten Gebieten im Vergleich zur unberührten Natur die zehnfache Menge an Fullerenen gefunden werden, die wahrscheinlich unbeabsichtigt durch Verbrennungsprozesse freigesetzt wurden .
Obwohl für den Nachweis von tatsächlich in der Umwelt vorhandene Mengen an Fullerenen bereits mehrere Messmethoden entwickelt wurden, sind nur wenige Studien verfügbar. Daher muss auf Computermodelle zurückgegriffen werden . Hier werden aus den Produktionsmengen die zu erwartenden Umweltkonzentrationen (PEC) berechnet, die klar eine Anreicherung von Fullerenen auf Deponien und in Kläranlagen vorhersagen . Aus den Kläranlagen können die Fulleren Nanomaterialien in Oberflächengewässer oder über die Klärschlammverbrennung in die Müllverbrennung gelangen.
Nach Auswertung verschiedener toxikologischer Studien lag der errechnete Risikoquotient für Fullerene unter 1, so dass bei den gegenwärtigen (theoretischen) Umweltkonzentrationen an Fullerenen keine Risiken für Umweltorganismen zu erwarten sind. Allerdings müssen diese theoretisch errechneten Werte zukünftig durch experimentell erhobene Messwerte bestätigt werden bzw. an steigende Produktionsmengen angepasst werden.
Ob und in welcher Form die Fullerene die Luft-Blut-Schranke überwinden, ist bis heute noch nicht final geklärt. Fullerene werden Kosmetika und Hautpflegeprodukten beigemischt. Sie dringen aber gezielt nur in die oberen Hautschichten und nicht in die tieferliegenden Schichten ein. Oberflächen-modifizierte Fullerene werden im Folgenden nicht berücksichtigt.
Aufnahme über die Lunge
Zum Beispiel können bei Verbrennungsprozessen entstandene Fullerene ähnlich wie andere natürliche oder synthetische Nanopartikel als Aerosol inhaliert werden. Allerdings sind die bei einer Verbrennung ungewollt entstandenen Mengen an Fullerenen sehr gering . Neben einzelnen freien Fullerenen können auch nanoskalige und bis zu 1 Mikrometer große Fulleren-Aggregate in die Lunge aufgenommen werden . Die Effizienz des Selbstreinigungsprozesses der Lunge scheint artspezifisch zu sein, da hier signifikante Unterschiede zwischen Maus und Ratte beobachtet werden konnten . Instillationsversuche von Fullerenen in Ratten zeigten eine leichte, vorübergehende Entzündungsreaktionen, jedoch keine Genotoxizität .
Basierend auf den bestehenden Erkenntnissen anderer kohlenstoffbasierter Nanomaterialien ist es für Fullerene grundsätzlich möglich, die Luft-Blut-Schranke zu überqueren. Allerdings geschieht dies nur in geringsten Mengen (unterhalb der Nachweisgrenze der heuten Analytik) .
Aufnahme über die Haut

Hautpflegecreme © vulkanismus / Fotolia.com
Ein Beispiel für die Verwendung von oberflächen-modifizierten Fullerenen in Kosmetika ist eine sog. Anti-Aging Creme einer japanischen Firma. Diese Creme enthält lipophile Partikel, die nur in die Oberhaut eindringen, nicht aber in die tieferliegende Lederhaut (vgl. Körperbarrieren – Nanopartikel und die Haut) . Über die Wirksamkeit der Fullerene als Anti-Aging Mittel liegen derzeit keine gesicherten Ergebnisse vor.
Laboruntersuchungen an Hautzelllinien zeigen, dass reine Fullerene keine toxischen Effekte auslösen, wenn sie vor der Verabreichung in verträglichen Lösungsmitteln (ohne Tetrahydrofuran) aufbereitet werden. Neben neuen Methoden helfen auch weitere chemische Modifikationen, die Dispergierbarkeit der Fullerene in wässrigen Lösungen zu verbessern. In der Regel wird dadurch kein zusätzliches toxikologisches Potenzial erzeugt, dennoch muss jede Fulleren-Variante derzeit separat geprüft werden .
Aufnahme über den Magen-Darm-Trakt
Die Tierstudie an Ratten hat aufgezeigt, dass nach oraler Gabe einer geringen Menge purer Fullerene nur ein leichter Anstieg der DNA Oxidation in Leber und Lunge, nicht aber im Magen-Darm-Trakt stattfand. Dieser Effekt scheint auch nur vorübergehend zu sein, da sich die Werte der Organe wenige Tage nach der Behandlung wieder normalisiert hatten .
Die große Vielfalt der Fullerene ermöglicht keine allgemeingültigen oder vergleichenden Aussagen zu ihrer Toxizität. Viele Organismen nehmen Fullerene in den Körper auf. Der Herstellungsprozess, insbesondere der Einsatz von Katalysatoren, und der Einsatz verschiedener Lösungsmittel beeinflussen die Toxizität oft zusätzlich, da auch diese Substanzen toxische Wirkungen haben können. Das macht es schwierig, die Effekte von denen reiner Fullerene klar abzugrenzen.
Bis 2010 wurde in vielen Fällen das Lösungsmittel Tetrahydrofuran (THF) verwendet, um Fullerene in wässrigen Medien gut zu verteilen, die für biologische Tests eingesetzt werden. Solche Suspensionen mit THF-gelösten Fullerenen zeigten toxische Effekte auf Umweltorganismen, die hauptsächlich auf Abbauprodukte des THFs in wässrigen Lösungen zurückzuführen waren . Lösungen mit Fulleren Nanomaterialien ohne Abbauprodukte verursachten keine negativen Effekte, weshalb seit 2010 größtenteils auf Lösungsmittel verzichtet wird und Alternativen wie Rühren oder Ultraschallbehandlung angewendet werden .
 Fullerene können von Fischen aus dem Wasser aufgenommen werden und bewirken art-spezifisch unterschiedliche Veränderungen wie Fettzusammensetzung, Kiemen-Struktur, Sterblichkeit und Störungen bei den Entwicklungsstufen. Ebenfalls beobachtet werden konnte eine Erhöhung von Stressgenen bei Embryonen des Zebrafisches sowie eine ausgelöste Immunreaktion bei Dickkopf-Elritzen Embryonen durch Fullerene, wobei Licht noch eine verstärkende Wirkung hatte .
Fullerene können von Fischen aus dem Wasser aufgenommen werden und bewirken art-spezifisch unterschiedliche Veränderungen wie Fettzusammensetzung, Kiemen-Struktur, Sterblichkeit und Störungen bei den Entwicklungsstufen. Ebenfalls beobachtet werden konnte eine Erhöhung von Stressgenen bei Embryonen des Zebrafisches sowie eine ausgelöste Immunreaktion bei Dickkopf-Elritzen Embryonen durch Fullerene, wobei Licht noch eine verstärkende Wirkung hatte .

In Blutzellen der Miesmuschel lösten Fullerene eine Entzündung aus, waren jedoch nicht akut toxisch. Im Gegensatz dazu wirken auch geringe Konzentrationen an Fulleren Nanomaterialen toxisch auf Auster-Embryonen, erwachsene Austern und isolierte Leberzellen. Allerdings wurde hier Toluol als Lösungsmittel verwendet, welches ähnliche Abbauprodukte wie THF bilden könnte .
 Bei Wasserflöhen bewirken hohe Dosen im Wasser verteilter Fullerene eine erhöhte Bewegungsaktivität und einem vermehrten Aufenthalt der Tiere an der Wasseroberfläche. Die Wasserflöhe wurden durch die Anwesenheit von Fullerenen nicht vergiftet, zeigten aber ein klares Fluchtverhalten. In einer weiteren Studie wurde ein verringertes Schwimmvermögen der Tiere beobachtet. Generell nehmen Wasserflöhe die Fullerene aus dem Wasser aktiv in den Darm auf. Sie gehen aber nicht in das Körpergewebe über und werden vermutlich wieder vollständig ausgeschieden . Alle beobachteten Verhaltensänderungen können jedoch ein wichtiger Hinweis auf eine Störung des Ökosystems sein. Bei Mückenlarven wurden von Entwicklungsverzögerungen ausgelöst durch Fullerene berichtet .
Bei Wasserflöhen bewirken hohe Dosen im Wasser verteilter Fullerene eine erhöhte Bewegungsaktivität und einem vermehrten Aufenthalt der Tiere an der Wasseroberfläche. Die Wasserflöhe wurden durch die Anwesenheit von Fullerenen nicht vergiftet, zeigten aber ein klares Fluchtverhalten. In einer weiteren Studie wurde ein verringertes Schwimmvermögen der Tiere beobachtet. Generell nehmen Wasserflöhe die Fullerene aus dem Wasser aktiv in den Darm auf. Sie gehen aber nicht in das Körpergewebe über und werden vermutlich wieder vollständig ausgeschieden . Alle beobachteten Verhaltensänderungen können jedoch ein wichtiger Hinweis auf eine Störung des Ökosystems sein. Bei Mückenlarven wurden von Entwicklungsverzögerungen ausgelöst durch Fullerene berichtet .
 Hohen Dosen von Fullerenen im Boden verursachen bei ausgewachsenen Regenwürmern eine geringere Fruchtbarkeit und Gewebeschäden der Haut und darunterliegenden Muskeln, haben jedoch keinen Einfluss auf die Sterblichkeit der Tiere. Dagegen sind jüngere Regenwürmer deutlich empfindlicher gegenüber Fullerenen. Sie zeigen ein verlangsamtes Wachstum und haben eine geringere Lebensdauer. Fadenwürmern reagierten in ähnlicher Weise. Sie zeigen eine verminderte Lebensfähigkeit, eine geringere Körpergröße und Fruchtbarkeit .
Hohen Dosen von Fullerenen im Boden verursachen bei ausgewachsenen Regenwürmern eine geringere Fruchtbarkeit und Gewebeschäden der Haut und darunterliegenden Muskeln, haben jedoch keinen Einfluss auf die Sterblichkeit der Tiere. Dagegen sind jüngere Regenwürmer deutlich empfindlicher gegenüber Fullerenen. Sie zeigen ein verlangsamtes Wachstum und haben eine geringere Lebensdauer. Fadenwürmern reagierten in ähnlicher Weise. Sie zeigen eine verminderte Lebensfähigkeit, eine geringere Körpergröße und Fruchtbarkeit .
 In Nutzpflanzen wie Zucchini oder Tomate wurde eine gesteigerte Aufnahme von Pestiziden nach Behandlung mit Fullerenen beobachtet. Vermutlich binden die Pestizide an die Fulleren Nanomaterialien und werden von diesen in die Pflanze transportiert. Bittermelonenpflanzen zeigten unter Einwirkung von Fullerol einen Anstieg der Biomasse, des Wassergehaltes sowie von Fruchtanzahl, –länge und –gewicht. In Wasserpflanzen und Algen verursachen Fullerene hingegen ein verringertes Wachstum .
In Nutzpflanzen wie Zucchini oder Tomate wurde eine gesteigerte Aufnahme von Pestiziden nach Behandlung mit Fullerenen beobachtet. Vermutlich binden die Pestizide an die Fulleren Nanomaterialien und werden von diesen in die Pflanze transportiert. Bittermelonenpflanzen zeigten unter Einwirkung von Fullerol einen Anstieg der Biomasse, des Wassergehaltes sowie von Fruchtanzahl, –länge und –gewicht. In Wasserpflanzen und Algen verursachen Fullerene hingegen ein verringertes Wachstum .
Fullerene haben auch antibakterielle Eigenschaften. Das bedeutet, dass Fullerene das Wachstum bestimmter Bakterien vermindern können .
Fullerene haben generell die Eigenschaft, andere Stoffe, z.B. Chemikalien sehr stark zu binden. Dadurch kann die Verfügbarkeit und Toxizität von Chemikalien in der Umwelt beeinflusst werden. Abhängig von der Art der Chemikalie kann sowohl eine Abschwächung als auch eine Verstärkung des toxischen Effektes in Algen und Wasserflöhen beobachtet werden . Daher sollte nicht nur die Toxizität von Fullerenen allein, sondern auch ihre Interaktion mit anderen in der Umwelt vorhandenen Substanzen berücksichtigt werden.
Abschließend lässt sich die Toxizität der Fullerene aufgrund ihrer Vielfältigkeit derzeit schwer beurteilen. Von sehr geringen Dosen, wie sie derzeit in der Umwelt zu erwarten sind, geht jedoch keine Gefahr für Umweltorganismen aus. Viele weitere Faktoren, wie z.B. die Rolle von Katalysatorrückständen und Verunreinigungen, müssen berücksichtigt werden.
Reine Fullerene verklumpen und können von verschiedenen Zelltypen aufgenommen werden. Einmal in der Blutbahn angelangt, können sich Fullerene im ganzen Körper verteilen. Oberflächen-modifizierte Fullerene werden im Folgenden nicht berücksichtigt.
Verhalten im Körper
Bei Ratten, welchen eine niedrige Dosis (0.64 mg/kg) nicht-modifizierter Fullerene über das Futter verabreicht wurden, konnten leichte Stresssymptome in der Leber und Lunge nachgewiesen werden. Dies ist ein indirekter Hinweis darauf, dass Fullerene über eine Aufnahme über den Magen-Darm-Trakt zu anderen Organen gelangen könnten . Der eindeutige Nachweis ist aber noch nicht erbracht.
Intravenöse Zugabe und Verteilung im Körper
Um die Verteilung der Partikel im Körper über den Blutstrom zu untersuchen, wurden radioaktiv markierte, nicht-modifizierte Fullerene in Ratten gespritzt. Die verabreichten Fullerene wurden in der Leber, der Lunge, aber auch in der Plazenta und im Fötus nachgewiesen. Ebenfalls erfolgte eine Weitergabe der Fullerene an die Nachkommen über die Muttermilch . Die im Versuch verabreichte Dosis von 0,3 mg 14C markierten Fullerenen pro kg Körpergewicht ist allerdings hoch und käme so in der Realität nicht vor. Dennoch bestätigt dieser Versuchsansatz, dass nicht alle biologischen Barrieren für so winzige Nanopartikel wie die Fullerene (0,7 nm) ein Hindernis sind. Ähnliche Ergebnisse sind auch bei menschlichen Plazenten gefunden worden .
Aufnahmeverhalten in Zellen
Eine Vielzahl von Zellen wie Makrophagen oder Epithelzellen sind in der Lage, Agglomerate von nicht-modifizierten Fullerenen von bis zu wenigen Mikrometern aufzunehmen. Allerdings lassen sich auf Kohlenstoff-basierende Nanomaterialien nur mit großem technischem Aufwand im Gewebe oder in Zellen nachweisen . Nach erfolgter Aufnahme in die Zelle sind die Fullerene in verschiedenen Zellorganellen wie Lysosomen, Endosomen oder im Zytosol zu finden. Hier lösen sie, wenn überhaupt, nur leichte vorübergehende Entzündungsreaktionen aus .
Obwohl sie nur aus einem Kohlenstoffgerüst bestehen, gibt es eine Vielzahl verschiedener Fullerene, die sich vor allem durch Modifikationen der Partikel-Oberfläche ergeben. Diese Modifikationen beeinflussen die Eigenschaften der Fullerene und damit auch ihr Umweltverhalten, so dass keine allgemeingültigen Aussagen beispielsweise hinsichtlich ihrer Mobilität getroffen werden können.

Wasser Probennahme © kozorog / fotolia.com
In Wasser bzw. wässrigen Medien lassen sich nicht-modifizierte Fullerene nur schlecht verteilen, was durch eine Veränderung der Oberfläche verbessert werden kann. Fulleren Nanomaterialien liegen selten einzeln, sondern meist agglomeriert, d.h. in Komplexen aus mehreren Fullerenen, vor.
Einen entscheidenden Einfluss auf die Stärke der Komplexbildung haben die Salzkonzentration, die Art des Salzes und der pH-Wert des Wassers. Auch natürliche organische Verbindungen beeinflussen den Agglomerationsprozess und verhindern sowohl die Zusammenlagerung der Fullerene als auch deren lichtabhängige Umwandlung .
Eine Bestrahlung mit UV-Licht (einem Anteil des Sonnenlichts) kann zu chemischen Veränderungen an der Oberfläche der Fullerene führen, und so den Verbleib und Transport der Fullerene in Gewässern beeinflusst. Fullerole, das sind mit Hydroxyl-Gruppen besetzte Fullerene, können sogar durch sehr lange Einwirkung von UV-Licht aufgelöst werden. Aufgrund ihrer schlechten Verteilbarkeit in Wasser lagern sich Fullerene bevorzugt auf dem Grund von Gewässern ab. Von dort können sie sich zum Teil durch die Bindung an natürlich vorkommende Partikel wieder im Wasser verteilen .

Pflanzen Keimungssequenz © weerapat1003 / fotolia.com
Auch die Zusammensetzung von Böden hat einen wesentlichen Einfluss auf die Verteilung der Fullerene, insbesondere Salzgehalt, pH-Wert, Temperatur und Feuchtegrad des Bodens. Die Fulleren Nanomaterialien liegen hauptsächlich als Agglomerate vor, wodurch sie zwar weniger beweglich sind, allerdings auch vermehrt im Boden vorhandene Schadstoffe binden und anreichern können. Je nach Beschaffenheit können die Fullerene zudem eine starke Bindung mit den Bodenkomponenten eingehen.
Generell sind Fullerene widerstandsfähig gegenüber Zersetzungsprozessen. Sie verbleiben daher lange Zeit in der Umwelt und können z.B. von Pflanzen aufgenommen werden. Bestimmte Pilze können Fullerole aufgrund ihrer veränderten Oberfläche abbauen .
Zusammenfassend können sich Fullerene gut oder schlecht in Wasser verteilen, was ihr Verhalten in Gewässern entscheidend beeinflusst. Zudem liegen sie oft nicht einzeln, sondern zusammengelagert zu Agglomeraten vor. Diese Faktoren erschweren den Vergleich zwischen den verschiedenen Fullerenen und allgemeingültige Aussagen über das Umweltverhalten sind schwer zu treffen.
 >
>