Kohlenstoff-Nanoröhrchen werden seit Ihrer Entdeckung 1991 als „Wundermaterial“ angesehen, da sie außergewöhnliche Eigenschaften besitzen: Sie sind stärker als Stahl, aber dabei sehr leicht. Je nach Art der Röhrchen leiten sie elektrischen Strom unterschiedlich gut, was sie auch für die Elektronikindustrie interessant macht. Der Umfang der aktuellen Produktion ist trotzdem noch sehr gering.

Hightech Fahrrad © Robert Neumann / fotolia.com
Wie könnte ich damit in Kontakt kommen?
Der direkte Kontakt mit Kohlenstoff-Nanoröhrchen dürfte für Verbraucher eher unwahrscheinlich sein. Denn das Material wird weltweit in äußerst geringen Mengen produziert und ist in nur wenigen Produkten, die sich auf dem Markt befinden, enthalten. Bisherige Anwendungen konzentrieren sich auf Verbundwerkstoffe oder Elektronikbauteile. Hier werden keine Röhrchen freigesetzt, so dass ein direkter Kontakt mit ihnen frühestens dann zu erwarten sein könnte, wenn die Produkte am Ende ihres Lebenszyklus entsorgt werden.
Wie gefährlich ist das Material für Mensch und Umwelt?
Die Röhrchen sind aufgrund ihrer langen, fadenartigen Form bereits in der Diskussion: Grundsätzlich stellen faserartige Materialien für die Lunge ein Problem dar, vor allem dann, wenn die Fasern eine Mindestlänge von 15 bis 20 Mikrometern besitzen (das entspricht einem Viertel bis zu einem Drittel des Durchmessers eines menschlichen Haares). Fasern mit dieser Länge sind bereits lange bekannt für ihre kritische Wirkung in der Lunge (siehe Asbestproblematik). Dies trifft auch auf Kohlenstoffnanoröhrchen zu, wenn diese Mindestlänge von 15 Mikrometern erreicht ist. Außerdem müssen sie noch sehr steif sein, denn nur dann können sie von den Reinigungsmechanismen der Lunge nicht beseitigt werden. Unter diesen Umständen führen sie zu einer Entzündung des Gewebes, was nach 20 bis 30 Jahren zu einer Tumorbildung führen kann.
Fazit
Durch die geringe Produktionsmenge gibt es derzeit keine Probleme für Mensch und Umwelt. Das könnte sich aber schnell ändern, wenn die weltweite Produktion massiv ansteigen sollte. Das dürfte davon abhängen, wie viele neue Produkte auf den Markt kommen, in denen die Röhrchen enthalten sind.
Nebenbei
Die Bayer AG hat im Jahr 2013 die Produktion der Kohlenstoff-Nanoröhrchen aus wirtschaftlichen Gründen eingestellt.
Eigenschaften und Anwendungen
Vor etwa 30 Jahren setzte die Entdeckung der fußballförmigen Fullerene eine neue Entwicklung in Gang, die zu nachhaltigen Einflüssen auf viele Bereiche in der Technik und im täglichen Leben führen wird. Denn nachdem man das „Bauprinzip“ verstanden hatte, entwickelten es die Forscher weiter. Das Ergebnis waren „verlängerte“ Fullerene, nämlich Kohlenstoff-Nanoröhrchen (engl. carbon nanotubes, CNT): Diese bilden neben Graphit, Diamant, Fullerenen und Graphen eine weitere Modifikation des Elements Kohlenstoff. Zudem sind Sie mittlerweile eines der wohl am meisten zitierten Nanomaterialien.
Interessant macht die CNTs vor allem ihr einzigartiges Eigenschafts- und Anwendungsspektrum: die Röhrchen sind sehr stabil. Die Zugfestigkeit einer mehrwandigen Kohlenstoff-Nanoröhre wurde zu 63GPa bestimmt, das entspricht etwa dem 50-fachen von Stahl, und dies bei deutlich geringerem Gewicht der CNTs. Sie können zudem isolierend, halbleitend oder metallisch leitend sein. Je nachdem, wie sie hergestellt werden, können ihre Eigenschaften direkt eingestellt werden.
So könnten sie für ein breit gefächertes Spektrum an Anwendungen von Nutzen sein, und in allen Industriezweigen hofft man auf innovative Hightech-Anwendungen mit CNTs. Beispiele hierfür sind Transistoren aus Nanoröhren, Nanoröhrenspeicher, Nanoröhren zur Verbesserung von Kunststoffen, für die Messtechnik. Doch das sind bei weitem nicht alle Anwendungsbereiche.
![Schematischer Überblick über die verschiedenen Struktur-Arten von Kohlenstoff-Nanoröhrchen: einwandig (SWCNT), mehrwandig (MWCNT) und auch mögliche Oberflächen-Modifikationen. © Angepasst mit Erlaubnis von Jackson, P et al. (2013). Bioaccumulation and ecotoxicity of carbon nanotubes. Chem Cent J, 7(1): 154. Open Access article [CC-BY-2.0 (http://creativecommons.org/licenses/by/2.0)]. Schematischer Überblick über die verschiedenen Struktur-Arten von Kohlenstoff-Nanoröhrchen: einwandig (SWCNT), mehrwandig (MWCNT) und auch mögliche Oberflächen-Modifikationen. © Angepasst mit Erlaubnis von Jackson, P et al. (2013). Bioaccumulation and ecotoxicity of carbon nanotubes. Chem Cent J, 7(1): 154. Open Access article [CC-BY-2.0 (http://creativecommons.org/licenses/by/2.0)].](http://iai-dana4.iai.kit.edu/wp-content/uploads/2020/10/CNT-Jackson-2013-DE.png)
Schematischer Überblick über die verschiedenen Struktur-Arten von Kohlenstoff-Nanoröhrchen: einwandig (SWCNT), mehrwandig (MWCNT) und auch mögliche Oberflächen-Modifikationen. © Angepasst mit Erlaubnis von Jackson, P et al. (2013). Bioaccumulation and ecotoxicity of carbon nanotubes. Chem Cent J, 7(1): 154. Open Access article [CC-BY-2.0 (http://creativecommons.org/licenses/by/2.0)] .
In sämtlichen Schlüsselbranchen unserer heutigen Technologiegesellschaft finden sich Einsatzmöglichkeiten oder gar bereits am Markt befindliche Produkte, so z.B. als Zusatz zu verschiedenen Kunststoffen im Bereich der Elektronik, im Automobilbau, im Leichtbau oder zur Herstellung von Sportgeräten. In Zukunft sollen CNTs dabei mithelfen, die Energiewende in Deutschland erfolgreich zu bewältigen, beispielsweise durch verbesserte Batterien, stabilere Rotorblätter von Windrädern oder durch die Anwendung in Solar- und Brennstoffzellen; aber auch in der Bauchemie, z. B. für Hochleistungsbeton, sollen sie Marktreife erlangen.
Die Vielfalt der möglichen Anwendungen birgt ein erhebliches wirtschaftliches Potential. Deshalb forschte in Deutschland 2008-2014 ein Wissenschaftsbündnis aus über 90 namhaften Partnern aus Forschung und Industrie in der Innovationsallianz Carbon Nanotubes (Inno.CNT) an der Weiterentwicklung von CNTs und Folgeprodukten. Dieses mit 90 Millionen Euro ausgestattete Bündnis wurde zur Hälfte von der Bundesregierung finanziert.
Die Kohlenstoff-Nanoröhrchen, die als einwandige (engl. single walled oder SW) CNTs mit einem Durchmesser von weniger als 5 nm vorliegen, oder als mehrwandige (engl. multi-walled oder MW) CNTs mit Durchmessern bis zu über 100 nm, werden jedoch nicht nur auf ihre potentiellen wirtschaftlichen Chancen hin untersucht. Kohlenstoff-Nanoröhren zeigen zudem aufgrund von Van-der-Waals-Kräften eine starke Tendenz sich zu Bündeln zu vereinigen.
Kohlenstoff-Nanoröhrchen sind nicht selbstentzündlich. Als fein verteilte Mischung mit Luft (Staub) unter Einwirkung einer Zündquelle sind Kohlenstoff-Nanoröhrchen entzündlich (Staubexplosion). Das Verhalten bei einer Staubexplosion ist vergleichbar mit dem anderer, kohlenstoffbasierter Materialien.
Herstellung
CNTs können über verschiedene Verfahren großtechnisch hergestellt werden, mittels Laserabtrag von Graphit, Lichtbogenentladung zwischen Kohlenstoffelektroden oder aber die chemische Gasphasenabscheidung (CVD). Hierbei werden Kohlenwasserstoffe katalytisch zersetzt und man kann CNTs weitgehend parallel auf einem Substrat „wachsen“ lassen. Hierbei ist insbesondere die Abtrennung der Katalysatoren nach dem Herstellungsprozess enorm wichtig um die Kohlenstoffnanoröhrchen anschließend für alle eingangs erwähnten Anwendung einsetzen zu können .
Trotz vieler Studien kann kein abschließendes Urteil über die Giftigkeit von Kohlenstoff-Nanoröhrchen gefällt werden, da die beobachteten Effekte in der Literatur sehr kontrovers diskutiert werden.
Untersuchungen am lebenden Organismus - in vivo
Angesichts möglicher gesundheitsschädigender Wirkungen, aber auch im Hinblick auf potenzielle medizinische Anwendungen ist die Untersuchung der Verteilung von Kohlenstoff-Nanoröhrchen im Körper (in vivo) von großem Interesse .
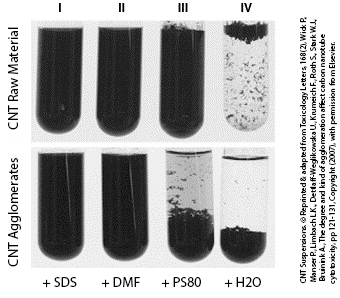
Unterschiedliche Suspensionen von Kohlenstiff-Nanoröhrchen. © Verwendet & angepasst aus Toxicology Letters, 168(2), Wick P., Manser P., Limbach L.K., Dettlaff-Weglikowska U., Krumeich F., Roth S., Stark W.J., Bruinink A., The degree and kind of agglomeration affect carbon nanotube cytotoxicity, pp 121-131, Copyright (2007), mit Erlaubnis von Elsevier .
Kohlenstoff-Nanoröhrchen (CNTs) werden in der Regel durch Inhalation, Instillation oder Aspiration in die Lungen von Versuchstieren gebracht. In mehrwöchigen Inhalationsstudien an Ratten mit mehrwandigen Kohlenstoff-Nanoröhrchen (engl. multi walled carbon nanotubes, MWCNTs) konnte keine systemische Toxizität nachgewiesen werden. Bei der Instillation und Aspiration werden die Nanopartikel zuerst in einer Flüssigkeit gelöst und dann in die Lunge bzw. auf der Zunge als Tropfen verabreicht und eingeatmet .
Die physiologische Relevanz dieser Methoden für die Lunge ist allerdings sehr fraglich, da es zum einen zur Aggregation der Nanomaterialien in der verabreichten Flüssigkeit kommt und zum anderen die komplette Dosis auf einmal verabreicht wird. Für eine abschließende Bewertung der Risiken einer Exposition mit Kohlenstoff-Nanoröhrchen unter realistischen Arbeitsplatz-Konzentrationen gibt es leider zurzeit nicht genügend Inhalationsstudien von unabhängigen Laboratorien.
In unterschiedlichen Studien wurden Kohlenstoff-Nanoröhrchen entweder in die Bauchhöhle, in die Venen oder auch in die Lunge von Versuchstieren eingespritzt. In diesen Fällen wurden die CNTs nach einiger Zeit in den Nieren, aber auch in der Milz, der Leber oder der Lunge gefunden. Häufig werden sie in den Organen durch dort vorhandene Makrophagen aufgenommen .
Bei einer Verabreichung über den Magen werden die Kohlenstoff-Nanoröhrchen innerhalb von 12 Stunden direkt über den Stuhl ausgeschieden wurde, ohne in den Blutkreislauf zu gelangen. Akute Giftigkeit konnte in dieser Studie, egal unter welchen Applikationsbedingungen, NICHT nachgewiesen werden . Allerdings gibt es kaum Studien zum Einfluss von Kohlenstoff-Nanoröhrchen auf die inneren Organe .
Darüber hinaus sind Kohlenstoff-Nanoröhrchen nicht gleich Kohlenstoff-Nanoröhrchen. Durch das An- und Einbringen von verschiedensten Funktionalisierungen, wie z.B. die Anbindung von Farbstoffen zum Sichtbarmachen im Mikroskop, verändern sich die Oberflächeneigenschaften der CNTs und somit auch ihr Verhalten im Körper (Verteilung und Verweildauer) . Über eine gezielte Veränderung der Oberfläche kann aber auch das Gefahrenpotential der Kohlenstoff-Nanoröhrchen kontrolliert „eingestellt" werden .
Durch die enorme Variation des Materials jedoch (Reinheit, Oberflächenbeschaffenheit, die verabreichte Dosis und ihr Agglomerationsstatus, d.h. wie stark kleben einzelne Kohlenstoff-Nanoröhrchen aneinander und bilden somit größere Partikel) sind auch die Resultate der Studien sehr unterschiedlich .
Die immense Verschiedenartigkeit der Kohlenstoff-Nanoröhrchen sowie Unterschiede in der Versuchsdurchführung und Analyse führen dazu, dass sich kein einheitliches Bild abzeichnet, wie sich die CNTs nach ihrer Aufnahme im Körper verhalten. Hier muss eine Vereinheitlichung der Versuchsprotokolle in Zukunft Abhilfe schaffen.
Untersuchungen außerhalb des Organismus - in vitro

Hellfeld-Bild von A549-Zellen, mit einwandigen Kohlenstoff-Nanoröhrchen (SWCNTs, markiert mit weißen Pfeilen) behandelt © Karin Pulskamp / FZK, 2009.
Alternativ zu in vivo Versuchen in Tiermodellen werden die Wirkungen von Kohlenstoff-Nanoröhrchen (CNTs) vielfach im Labor in Zellkultur-Versuchen (in vitro) untersucht. Dafür werden die CNTs in eine Flüssigkeit eingebracht (suspendiert) und dann dem Zellkulturmedium beigefügt, so dass es zu einem Kontakt zwischen den Zellen und den CNTs (Exposition) kommt. Über die letzten Jahre wurden sehr viele solcher in vitro Studien durchgeführt. Trotzdem kann kein abschließendes Urteil über die Toxizität der CNTs gefällt werden, dafür waren die getesteten Kohlenstoff-Nanoröhrchen und angewandten Testmethoden zu unterschiedlich.
Einige Schlüsse aus den publizierten Studien lassen sich aber dennoch ziehen: z.B. dass die Bündelung der Kohlenstoff-Nanoröhrchen (Agglomeration) ihre schädliche Wirkung erhöhen kann . Aber diese langen oder agglomerierten CNTs können nur bedingt eingeatmet werden, da sie viel zu groß sind, um in die Lunge zu gelangen. Auch sind viele der berichteten toxischen Wirkungen der Kohlenstoff-Nanoröhrchen auf die extrem hohen eingesetzten Dosen der Nanomaterialien zurückzuführen, die z.T. nicht einmal bei einer technischen Störung während der Produktion erreicht werden könnten.

TEM-Aufnahme von Kohlenstoff-Nanoröhrchen (CNTs). © Verwendet mit Erlaubnis von Woerle-Knirsch, JM et al. (2006). Oops they did it again! Carbon nanotubes hoax scientists in viability assays. Nano Lett, 6(6): 1261-12. Copyright (2013) © American Chemical Society .
Häufig sind die Kohlenstoff-Nanoröhrchen nach ihrer Produktion noch mit vielen Verunreinigungen belastet. Das können Katalysatormetalle sein (häufig Eisen, aber auch Nickel, Cobalt oder Molybdän), amorpher Kohlenstoff (ähnlich wie er im Feinstaub vorliegt) oder andere Zusatzstoffe. Es wurde nachgewiesen, dass akute Wirkungen im Wesentlichen von diesen Verunreinigungen ausgehen können .
Kohlenstoff-Nanoröhrchen gelten als sehr stabil und biopersistent. Trotzdem konnte ein enzymatischer Abbau von funktionalisierten und auch nicht-funktionalisierten einwandigen CNTs im Experiment nachgewiesen werden . Auch die Fresszellen waren bei in vitro Versuchen in der Lage, die einwandigen Kohlenstoff-Nanoröhrchen abzubauen .
Um Kohlenstoff-Nanoröhrchen in der Medizin einsetzen zu können, z.B. als Transporter für Wirkstoffe oder Medikamente, müssen die CNTs oft chemisch verändert werden (vgl. Querschnittsthemen – Beschichtungsformen von Nanomaterialien). Entsprechend angepasst sind die Kohlenstoff-Nanoröhrchen daraufhin z.B. wasserlöslich und wirken nicht mehr akut toxisch .
Um sinnvolle und fundierte Schlussfolgerungen zur Toxizität von Kohlenstoff-Nanoröhrchen treffen zu können, sollten neben einer umfassenden Materialcharakterisierung auch umweltrelevante Dosen, eine angepasste Darreichungsform sowie realitätsnahe und geeignete Messmethoden zum Einsatz kommen . In Zukunft gilt es, passende Modelle zu entwickeln, die zum einen die Ergebnisse von vergleichenden in vitro und in vivo Studien analysieren und zum anderen die genetische Antwort (Ein- und Ausschalten von Genen oder Genprogrammen) der Zellen oder des Organismus erfassen und charakterisieren helfen. Dank solcher Modelle sollte es dann möglich sein, die Toxizität einer bestimmten Substanz bzw. eines Nanomaterials vorherzusagen . Standardisierte Arbeitsanleitungen inklusive international anerkannte Referenzmaterialien würden die Qualität und Vergleichbarkeit der in vitro Studien deutlich verbessern .
Kohlenstoff-Nanoröhrchen bestehen ausschließlich aus Kohlenstoff, einem Element welches in allen Lebewesen und der Luft vorkommt. Diese Tatsache erschwert den Nachweis in der Umwelt. Derzeit gibt es keine Angaben zu den tatsächlich vorhandenen Mengen an Kohlenstoff-Nanoröhrchen in der Umwelt und ihrer Verteilung in den einzelnen Kompartimenten (z.B. Wasser, Boden).
Ein wichtiger Punkt für die Abschätzung einer möglichen Gefährdung für Organismen ist die Bestimmung der tatsächlich auftretenden oder zu erwartenden Konzentrationen von Nanomaterialien in der Umwelt. Wenn zum Beispiel nur bei sehr hohen Konzentrationen toxische Effekte auftreten, in der Realität (in der Umwelt) aber nur ein Bruchteil dessen gefunden werden kann, dann sind schädigende Effekte eher unwahrscheinlich, es besteht also keine Gefahr für die Umwelt.

© spuno / fotolia.com
Aus Mangel an experimentellen Daten simulieren die Forscher die Verteilung der Nanomaterialien in der Umwelt mit Hilfe spezieller Computerprogramme, um anschließend mögliche zu erwartende Umwelt-Konzentrationen (PEC-Wert) vorhersagen bzw. berechnen zu können. Als Ausgangspunkt für diese Berechnungen werden die Produktionsmengen von Kohlenstoff-Nanoröhrchen verwendet. Da CNTs hauptsächlich als Verbundstoffe eingesetzt werden, gelangt nur ein sehr geringer Anteil direkt in Luft oder Wasser. Der Großteil wird entweder auf Mülldeponien oder in Müllverbrennungsanlagen entsorgt. Vergleicht man die berechneten Umwelt-Konzentrationen mit den gefährlichen Konzentrationen, so zeigt sich gegenwärtig, dass von Kohlenstoff-Nanoröhrchen keine Risiken für Umweltorganismen zu erwarten sind .
Auch für Anwendungen wie Batterien oder Textilien können Kohlenstoff-Nanoröhrchen eingesetzt werden. Ergebnisse der Computersimulationen für diese Fallbeispiele haben ergeben, dass die CNTs mit hoher Wahrscheinlichkeit nicht nur während der Herstellung, sondern auch bei Gebrauch und Entsorgen der Produkte freigesetzt werden können . Beispielsweise können bei unvollständiger Verbrennung von entsorgten CNT-haltigen Produkte geringe Mengen der Kohlenstoff-Nanoröhrchen in die Umwelt gelangen. Vergleicht man für diese Beispiele die möglichen erreichbaren Umweltkonzentrationen von Kohlenstoff-Nanoröhrchen mit einem anderen kohlenstoff-basierten Material wie Industrieruß, dann werden die berechneten Mengen für die CNTs als sehr gering eingeschätzt .
Allerdings müssen diese berechneten Werte in Zukunft durch tatsächliche Messwerte bestätigt bzw. an steigende Produktionsmengen angepasst werden. Erste methodische Ansätze für den direkten Nachweis von Kohlenstoff-Nanoröhrchen in der Umwelt wurden bereits entwickelt .
Da Kohlenstoff-Nanoröhrchen derzeit weder in Nahrungsmitteln noch in kosmetischen Produkten eingesetzt werden, ist die Aufnahme über die Lunge, z.B. bei der Produktion, die wahrscheinlichste Eintrittsart in den Körper. Studien mit Labortieren haben gezeigt, dass Kohlenstoff-Nanoröhrchen in Abhängigkeit von der Größe bis in die tiefen Regionen der Lunge vordringen können.
Aufnahme über die Lunge - Inhalation
In der Mehrzahl der Studien werden die Kohlenstoff-Nanoröhrchen den Versuchstieren auf einem ungewöhnlichen Weg verabreicht, was die Frage nach der Relevanz der Ergebnisse für das tägliche Leben aufwirft. So werden Kohlenstoff-Nanoröhrchen z.B. durch das Einflößen einer kleinen Menge einer hochdosierten flüssigen Suspension von Nanomaterialien durch die Luftröhre direkt in die Lungenbläschen (Instillation) oder mittels Einsaugen einer Nanopartikel-enthaltenden Flüssigkeit durch den Rachen (Aspiration) verabreicht. Beide Zufuhrwege entsprechen nicht den z.B. am Arbeitsplatz vorkommenden luftgetragenen (Nano)Partikeln, die ähnlich wie Feinstaub eingeatmet werden könnten.
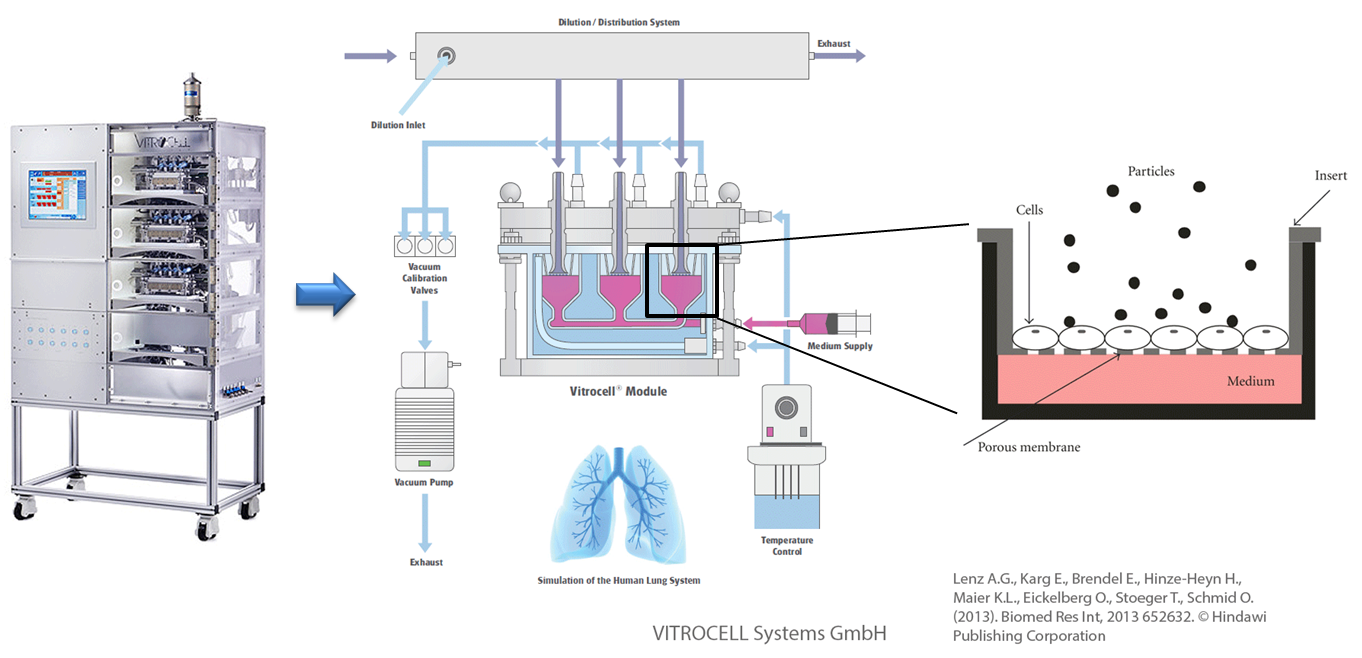
In vitro Exposition an der Luft-Flüssigkeits-Grenzschicht (ALI) am Beispiel des Karlsruhe Expositionssystems. Verwendet und angepasst mit Erlaubnis von © Vitrocell Systems GmbH, Lenz A.G., Karg E., Brendel E., Hinze-Heyn H., Maier K.L., Eickelberg O., Stoeger T., Schmid O. (2013). Biomed Res Int, 2013 652632. © Hindawi Publishing Corporation
In neueren Inhalationsstudien werden Kohlenstoff-Nanoröhrchen den Tieren über die Atemluft als Aerosol verabreicht, was eher der realen Situation entspricht. Diese Studien an Mäusen haben gezeigt, dass auch Kohlenstoff-Nanoröhrchen bis in die tiefsten Regionen der Lunge vordringen können .
Die Ergebnisse der verschiedenen Studien sind teilweise widersprüchlich und werden noch kritisch diskutiert. Manche Forschergruppen beobachten Stressreaktionen im Lungengewebe, bei denen es zu Entzündungsreaktionen in der Lunge, der Bildung von Granulomen und einer Veränderungen der Lungenfunktion kam. Ergebnisse aus anderen Studien hingegen beschreiben eine veränderte systemische Immunreaktionen (z.B. in der Milz und in Lymphknoten) ohne Veränderungen in der Lunge .

Arbeitsschutz. © Empa, 2009.
Erklären lassen sich die unterschiedlichen Ergebnisse über die verschiedenen Formen (Modifizierungen) der eingesetzten CNTs, der unterschiedlichen Verabreichungsmethode, sowie Variationen in der Dauer der Studien und der verabreichten Dosis. Trotz dieser Einschränkungen weiß man heute aber, dass dünne, lange, biopersistente, faserförmige Nanomaterialien pathogene Effekte (z.B. Entzündungen und Tumoren) auslösen können . Aus Sicherheitsgründen werden deshalb solche Kohlenstoff-Nanoröhrchen nicht mehr verwendet .
Bislang existieren noch sehr wenige Daten über die Konzentrationen von Kohlenstoff-Nanoröhrchen an industriellen Arbeitsplätzen. Erste Labor-Messungen konnten CNTs unter entsprechenden Versuchsbedingungen in der Luft nachweisen (ca. 0,7-53 µg/m3) . Durch die korrekte Anwendung von Vorsichtsmaßnahmen wie der Verwendung eines Labor-Abzugs und Schutzkleidung (Handschuhe, Atemmaske) kann eine Aufnahme von ungewünschten Nanomaterialien stark reduziert werden.
Allerdings fehlt gerade für CNTs noch der Nachweis, dass auch die kritischen großen und langen Fraktionen der Kohlenstoff-Nanoröhrchen in die Lunge aufgenommen werden können.
Aufnahme über die Haut - Dermal

© H.Bauer / fotolia.com
Eine gesunde intakte Haut bildet eine sehr effektive mechanische Barriere gegen Nanopartikel (vgl. Körperbarrieren – Nanopartikel und die Haut), was auch im Europäischen Projekt NanoDerm für Titandioxid-Partikel gezeigt werden konnte . Ein Transfer von Nanopartikel über die Haut in die Blutgefäße konnte bis heute nicht nachgewiesen werden. Ob Kohlenstoff-Nanoröhrchen (CNTs) über die Haut aufgenommen werden können, wurde bis jetzt noch nicht untersucht.
Allerdings kann hier ein Analogieschluss helfen:
Tätowierungsfarbe, insbesondere Schwarz, enthält Kohlenstoff-Partikel und diese Farbe wird mechanisch über eine Nadel in die tiefen Hautschichten deponiert. Nur wenige dieser Kohlenstoff-Partikel werden in die naheliegenden Lymphgefäße transportiert, die meisten bleiben an Ort und Stelle, wodurch sich die lebenslange Haltbarkeit der tätowierten Bilder erklärt.
Kohlenstoff-Nanoröhrchen sind in Bezug auf ihre Oberflächencharakteristik diesen Partikeln sehr ähnlich, so dass auch im Falle von CNTs von einem schlechten Transport ausgegangen werden kann.
Aufnahme über den Magen-Darm-Trakt
Kohlenstoff-Nanoröhrchen (CNTs) sind nicht für den Einsatz in Lebensmitteln zugelassen und es ist auch nicht absehbar, dass es Anwendungen in Lebensmitteln geben wird. Dennoch wäre es denkbar, dass z.B. eingeatmete Kohlenstoff-Nanoröhrchen durch Abhusten und Verschlucken in den Magen-Darm-Trakt gelangen und von dort weiter im Körper verteilt werden könnten. Bislang existieren jedoch nur wenige Analysen zu diesem Thema.
Nach der direkten Verabreichung von wasserlöslichen Kohlenstoff-Nanoröhrchen in den Magen von Mäusen hielten sich die CNTs nur für sehr kurze Zeit im Magen-Darm-Trakt auf und wurden innerhalb von 12 Stunden mit dem Stuhl ausgeschieden. Die Kohlenstoff-Nanoröhrchen gelangten nicht in die Blutbahn und es konnten auch keine biologischen Effekte beobachtet werden . Im Falle von kurzen oder langen mehrwandigen Kohlenstoff-Nanoröhrchen (engl. multi walled carbon nanotubes, CNTs), die direkt in den Magen von Mäusen gegeben wurden, traten nur bei den langen und steifen faserförmigen CNTs Entzündungen und Schäden der oberen Zellschichten auf. Diese beobachteten Effekte (pathogenen Reaktionen) sind schon seit längerem insbesondere für lange steife Asbest-Fasern bekannt .
Werden hingegen unveränderte Kohlenstoff-Nanoröhrchen direkt in die Blutbahn der Versuchstiere gespritzt, dann verteilen sie sich in verschiedenen inneren Organen (z.B. Leber, Milz, Lunge) und werden nur zu geringen Teilen über den Urin und Stuhl wieder ausgeschieden .
Auch für den Magen-Darm-Trakt kann ähnlich wie zur Aufnahme von CNTs über die Lunge kein abschließendes Fazit gezogen werden. Das Verhalten von Kohlenstoff-Nanoröhrchen hängt auch hier stark von ihrer jeweiligen Veränderung, der Art ihrer Verabreichung und ihrer Dosierung ab.
Der Begriff Kohlenstoff-Nanoröhrchen (CNTs) umfasst eine Gruppe Kohlenstoff-haltiger Nanomaterialien mit verschiedensten Eigenschaften, welche sich z.B. in der Art der Oberfläche oder in der Anzahl der Wände voneinander unterscheiden. Diese Merkmale beeinflussen auch wesentlich die Stärke der toxischen Wirkungen der CNTs. Viele der beobachteten Effekte werden auf die Faser-Form der Kohlenstoff-Nanoröhrchen zurückgeführt, die indirekte Effekte nach Kontakt mit der Oberfläche der Umweltorganismen auslösen kann. Allgemeingültige Aussagen zur Umwelttoxizität von Kohlenstoff-Nanoröhrchen sind bisher nicht möglich .
Kohlenstoff-Nanoröhrchen verursachen aufgrund ihrer Faser-Form indirekte toxische Effekte in Bakterien, indem sie wie Nadeln wirken und deren Zellhülle durchstechen und so mechanisch schädigen können. Über diesen Defekt in der Hülle wird das Wachstum der Bakterien stark eingeschränkt bzw. gänzlich gehemmt. Dieser Effekt auf Bakterien ist umso stärker, je besser die CNTs in der Nährlösung verteilt und vereinzelt sind .
 Einzellige Lebewesen, wie z.B. Wimperntierchen und Amöben, kommen in allen Gewässern vor und nehmen CNTs nachweislich auf, können diese aber auch wieder ausscheiden. Ihre Lebensfähigkeit wird durch die Kohlenstoff-Nanoröhrchen nicht beeinflusst, jedoch können sie ihre Nahrung (Bakterien) schlechter aufnehmen und verdauen .
Einzellige Lebewesen, wie z.B. Wimperntierchen und Amöben, kommen in allen Gewässern vor und nehmen CNTs nachweislich auf, können diese aber auch wieder ausscheiden. Ihre Lebensfähigkeit wird durch die Kohlenstoff-Nanoröhrchen nicht beeinflusst, jedoch können sie ihre Nahrung (Bakterien) schlechter aufnehmen und verdauen .
 Verschiedene Algenarten werden ebenfalls indirekt durch Kohlenstoff-Nanoröhrchen beeinflusst. Reine und beschichtete CNTs hemmen beispielsweise das Wachstum der Algen durch Abschirmung der Sonneneinstrahlung (Abschattung) oder durch die Bildung von Agglomeraten aus Algen und CNTs . Fehlt den Algen das lebensnotwendige Licht, kann die Zelle weniger Energie produzieren und das Wachstum wird gehemmt. Andere Einflussfaktoren wie z.B. die Beschaffenheit der Oberfläche der CNTs oder auch der Agglomerationsstatus in der wässrigen Umgebung haben kaum einen Einfluss auf das Algenwachstum . Zusätzlich können die Kohlenstoff-Nanoröhrchen auch oxidativen Stress in den Algen auslösen .
Verschiedene Algenarten werden ebenfalls indirekt durch Kohlenstoff-Nanoröhrchen beeinflusst. Reine und beschichtete CNTs hemmen beispielsweise das Wachstum der Algen durch Abschirmung der Sonneneinstrahlung (Abschattung) oder durch die Bildung von Agglomeraten aus Algen und CNTs . Fehlt den Algen das lebensnotwendige Licht, kann die Zelle weniger Energie produzieren und das Wachstum wird gehemmt. Andere Einflussfaktoren wie z.B. die Beschaffenheit der Oberfläche der CNTs oder auch der Agglomerationsstatus in der wässrigen Umgebung haben kaum einen Einfluss auf das Algenwachstum . Zusätzlich können die Kohlenstoff-Nanoröhrchen auch oxidativen Stress in den Algen auslösen .
 Bringt man die Kohlenstoff-Nanoröhrchen in den Boden von verschiedenen Nutzpflanzen wie z.B. Weizen oder Raps ein, nehmen die Pflanzen über ihre Wurzeln nur sehr geringe Mengen der angebotenen CNTs (0,005 %) auf . Das Wachstum der Pflanzen wurde nicht beeinflusst, so dass eine Anreicherung von CNTs in der Nahrungskette über Nutzpflanzen eher unwahrscheinlich ist. Bei Tomatenpflanzen konnten die aufgenommenen Kohlenstoff-Nanoröhrchen in Wurzeln, Sprossen und Früchten nachgewiesen werden. Außerdem wurden über die Kohlenstoff-Nanoröhrchen Stress-Gene in den Pflanzenzellen aktiviert, was auf einen erhöhten Stress für die Pflanze hinweist . Möglicherweise versucht die Pflanze aktiv, die CNTs wieder auszuscheiden. Bislang ist aber noch nicht geklärt, auf welchem Wege die Kohlenstoff-Nanoröhrchen Stress in den Pflanzenzellen auslösen.
Bringt man die Kohlenstoff-Nanoröhrchen in den Boden von verschiedenen Nutzpflanzen wie z.B. Weizen oder Raps ein, nehmen die Pflanzen über ihre Wurzeln nur sehr geringe Mengen der angebotenen CNTs (0,005 %) auf . Das Wachstum der Pflanzen wurde nicht beeinflusst, so dass eine Anreicherung von CNTs in der Nahrungskette über Nutzpflanzen eher unwahrscheinlich ist. Bei Tomatenpflanzen konnten die aufgenommenen Kohlenstoff-Nanoröhrchen in Wurzeln, Sprossen und Früchten nachgewiesen werden. Außerdem wurden über die Kohlenstoff-Nanoröhrchen Stress-Gene in den Pflanzenzellen aktiviert, was auf einen erhöhten Stress für die Pflanze hinweist . Möglicherweise versucht die Pflanze aktiv, die CNTs wieder auszuscheiden. Bislang ist aber noch nicht geklärt, auf welchem Wege die Kohlenstoff-Nanoröhrchen Stress in den Pflanzenzellen auslösen.
 Wasserflöhe nehmen Kohlenstoff-Nanoröhrchen unabhängig von ihrer Oberflächenladung auf und scheiden sie auch gleichermaßen wieder aus . Generell trägt der Ladungszustand der Oberfläche von Nanomaterialien entscheidend zum Verhalten der CNTs in wässrigem Milieu (Stabilität, Agglomeration) bei und kann so verschiedene Parameter wie Aufnahme oder Verteilung beeinflussen. In dieser Studie konnten die beobachteten Unterschiede in der Stärke der toxischen Effekte jedoch nicht auf die Aufnahme, sondern eher auf die Beschichtung der Kohlenstoff-Nanoröhrchen zurückgeführt werden .
Wasserflöhe nehmen Kohlenstoff-Nanoröhrchen unabhängig von ihrer Oberflächenladung auf und scheiden sie auch gleichermaßen wieder aus . Generell trägt der Ladungszustand der Oberfläche von Nanomaterialien entscheidend zum Verhalten der CNTs in wässrigem Milieu (Stabilität, Agglomeration) bei und kann so verschiedene Parameter wie Aufnahme oder Verteilung beeinflussen. In dieser Studie konnten die beobachteten Unterschiede in der Stärke der toxischen Effekte jedoch nicht auf die Aufnahme, sondern eher auf die Beschichtung der Kohlenstoff-Nanoröhrchen zurückgeführt werden .
 In Regenwürmern wurde ebenfalls die Wirkung von Kohlenstoff-Nanoröhrchen mit verschiedenen Oberflächenladungen verglichen . Ebenso wie im Wasser ändert sich auch das Verhalten der CNTs im Boden abhängig von den jeweiligen Oberflächeneigenschaften. Ähnlich der Wasserflöhe hatte auch das unterschiedliche Verhalten im Boden keinen Einfluss auf Aufnahme und Ausscheidung der Kohlenstoff-Nanoröhrchen in Regenwürmern. Zu toxischen Effekten in Würmern liegen derzeit keine Aussagen vor.
In Regenwürmern wurde ebenfalls die Wirkung von Kohlenstoff-Nanoröhrchen mit verschiedenen Oberflächenladungen verglichen . Ebenso wie im Wasser ändert sich auch das Verhalten der CNTs im Boden abhängig von den jeweiligen Oberflächeneigenschaften. Ähnlich der Wasserflöhe hatte auch das unterschiedliche Verhalten im Boden keinen Einfluss auf Aufnahme und Ausscheidung der Kohlenstoff-Nanoröhrchen in Regenwürmern. Zu toxischen Effekten in Würmern liegen derzeit keine Aussagen vor.

Die Larven des Afrikanischen Krallenfrosches reagieren akut toxisch auf Kohlenstoff-Nanoröhrchen. Die CNTs „verstopfen" die Kiemen und den Darm, so dass das Wachstum und somit auch die Überlebensfähigkeit der Larven stark eingeschränkt wird . Genotoxische Effekte wurden nicht beobachtet.
 Gibt man einwandige Kohlenstoff-Nanoröhrchen in das Futter von Regenbogenforellen, so nehmen diese die CNTs zwar auf, aber sie wirken nicht schädlich . Werden die Kohlenstoff-Nanoröhrchen jedoch direkt dem Wasser anstelle des Futters beigemischt, dann zeigen die Forellen eine Reizung der Kiemen und eine beschleunigte Atmung . Ähnlich wie bei den Froschlarven verstopfen die CNTs aufgrund ihrer Faserform die Kiemen der Fische und verursachen so die beobachteten Effekte.
Gibt man einwandige Kohlenstoff-Nanoröhrchen in das Futter von Regenbogenforellen, so nehmen diese die CNTs zwar auf, aber sie wirken nicht schädlich . Werden die Kohlenstoff-Nanoröhrchen jedoch direkt dem Wasser anstelle des Futters beigemischt, dann zeigen die Forellen eine Reizung der Kiemen und eine beschleunigte Atmung . Ähnlich wie bei den Froschlarven verstopfen die CNTs aufgrund ihrer Faserform die Kiemen der Fische und verursachen so die beobachteten Effekte.
Funktionalisierte, mehrwandige Kohlenstoff-Nanoröhrchen, die in Embryonen des Zebrabärblings injiziert wurden, sind nach 4 Tagen nicht mehr im Tier nachzuweisen und wurden demnach effektiv ausgeschieden . Die weitere Entwicklung der Fischembryonen wurde nicht beeinträchtigt. Allerdings waren bei der nachfolgenden Generation die Überlebensraten deutlich gemindert.
Betrachtet man den gesamten Lebenszyklus der Kohlenstoff-Nanoröhrchen - von der Herstellung und Verwendung bis hin zur Entsorgung – dann hat die Herstellung der CNTs einen wesentlich größeren Einfluss auf die Umweltorganismen als eine direkte Freisetzung der CNTs in die Umwelt . Beispielsweise können die vorher beschriebenen indirekten Effekte auf die Umweltorganismen durch Umweltschäden verursacht werden, die durch Abbau der Rohstoffe auftreten können oder aber auf die entstanden Abgase zurückzuführen sind.
Abschließend lässt sich die Toxizität von Kohlenstoff-Nanoröhrchen aufgrund ihrer Vielfältigkeit derzeit schwer beurteilen. Mechanische, indirekte Effekte aufgrund der Faser-Form werden in vielen Organismen beobachtet, insbesondere in Studien, bei denen sehr hohe Dosen getestet werden. Von sehr geringen Konzentrationen, wie sie derzeit in der Umwelt zu erwarten sind, geht nach derzeitiger Einschätzung keine Gefahr für Umweltorganismen aus.
Kohlenstoff-Nanoröhrchen werden vom Körper je nach Art der Verabreichung und Typ (einwandig, mehrwandig, modifiziert) aufgenommen und lassen sich in verschiedenen Organen und Zelltypen wiederfinden.
Verhalten im Körper
Kohlenstoff-Nanoröhrchen verhalten sich typischerweise wie Faser-förmige Stoffe, jedoch spielt hier die Länge der einzelnen Fasern eine bedeutende Rolle. Eine Aufnahme der CNTs über die Lunge ist nach allen derzeitigen Studien der kritischste Eintrittsweg in den Körper, da die Fasern länger in der Lunge verweilen als z.B. partikelförmige Materialien. Entscheidendes Merkmal ist dabei das Verhältnis von Durchmesser zu der Länge der CNT-Fasern .
Ab einer gewissen Länge können die Kohlenstoff-Nanoröhrchen genau wie andere faserförmige Schadstoffe nicht mehr von den normalen Reinigungsprozessen der Lunge entfernt werden. Die Fasern bleiben viel länger im Lungengewebe stecken, was zu einer dauerhaften Reizung des Gewebes führt. Dies kann sogar soweit gehen, dass die Fasern in tiefere Gewebeschichten „wandern" und dort über Jahre und Jahrzehnte eine Entzündungsreaktion auslösen, die schlussendlich die Bildung von Tumorbildung auslösen kann . Dies steht in Einklang mit Ergebnissen einer aktuellen Studie in Ratten, welche genau diesen Zusammenhang zwischen der Länge der Kohlenstoff-Nanoröhrchen und deren Wirkung auf die Bildung von Granulomen bei den behandelten Tieren gezeigt hatte .
Aufgrund dieser Effekte erklärt sich auch der Vergleich mit den Asbestfasern, wobei dies nur für die wirklich sehr langen Fasern (>5-10 µm) zutrifft. Kurze Kohlenstoff-Nanoröhrchen haben diesen Effekt nicht und können daher gut für technische Anwendungen eingesetzt werden .
Verhalten an der Blut-Hirn-Schranke
Preparation of injectable medicines. © sudok1 / fotolia.com
Eine einzige Studie hat bisher gezeigt, dass unveränderte, wasserunlösliche Kohlenstoff-Nanoröhrchen in geringen Mengen im Gehirn nachgewiesen werden können, nachdem sie direkt in die Blutbahn von Versuchstieren gespritzt wurden. Diese Beobachtung deutet darauf hin, dass Kohlenstoff-Nanoröhrchen unter bestimmten Bedingungen die Blut-Hirn-Schranke passieren können .
Allerdings wurde bislang noch keine Bestätigung dieser Studie für dieses Verteilungsverhalten veröffentlicht, in welcher zudem eine relativ große Dosis an CNTs eingesetzt wurde und auch die Untersuchung des Hirngewebes nicht genau beschrieben wurde. Es ist durchaus denkbar, dass kleine Bündel der CNTs in den Hirnkapillaren feststecken und dadurch dem Gehirn zugeordnet werden, obwohl sie die Gefäße gar nicht verlassen haben.
Hier muss noch abgewartet werden, ob andere Studien dieses Verhalten bestätigen und unter welchen genauen Bedingungen der Übertritt von Kohlenstoff-Nanoröhrchen aus dem Blut in das Gehirn möglich ist. Daraus könnten sich durchaus positive (z.B. Medikamentengabe im Gehirn) aber auch negative Auswirkungen (z.B. Zelltod, Hirnschädigung) ergeben, was allerdings noch genauer untersucht werden muss.
Aufnahmeverhalten in Zellen
![Paradigma der frustrierten Phagozytose für Asbest-Fasern und Kohlenstoff-Nanoröhrchen. © Verwendet & Angepasst mit Erlaubnis von Donaldson, K et al. (2010). Asbestos, carbon nanotubes and the pleural mesothelium: a review of the hypothesis regarding the role of long fibre retention in the parietal pleura, inflammation and mesothelioma. Part Fibre Toxicol, 7 5. Open Access article [CC-BY-2.0 (http://creativecommons.org/licenses/by/2.0)]. Paradigma der frustrierten Phagozytose für Asbest-Fasern und Kohlenstoff-Nanoröhrchen.](http://iai-dana4.iai.kit.edu/wp-content/uploads/2020/10/Donaldson-2010_DE-web.png)
Paradigma der frustrierten Phagozytose für Asbest-Fasern und Kohlenstoff-Nanoröhrchen. © Verwendet & Angepasst mit Erlaubnis von Donaldson, K et al. (2010). Asbestos, carbon nanotubes and the pleural mesothelium: a review of the hypothesis regarding the role of long fibre retention in the parietal pleura, inflammation and mesothelioma. Part Fibre Toxicol, 7 5. Open Access article [CC-BY-2.0 (http://creativecommons.org/licenses/by/2.0)] .
Ohne Stabilisierung mit Hilfsstoffen verklumpen Nanomaterialien bzw. Kohlenstoff-Nanoröhrchen (CNTs) sehr schnell. Da diese Verklumpungen (Agglomerate) größer als eine ganze Zelle sein können, ist es unter solchen Bedingungen eher unwahrscheinlich, dass die Zellen Kohlenstoff-Nanoröhrchen aufnehmen oder sie "ersticken" daran (frustrierte Phagozytose).
Kleinere Agglomerate werden durch die Zellen via Pinozytose aufgenommen und können mittels Elektronenmikroskopie in Zelleinschlüssen (sogenannten Vesikeln) nachgewiesen werden. Die Vesikel-Membran schützt die restlichen Zellkomponenten vor den Kohlenstoff-Nanoröhrchen, d.h. diese befinden sich zwar in der Zelle, dort aber immer noch abgekapselt Eine Studie zeigt aber, dass durchaus die Möglichkeit besteht, dass CNTs aus solchen Einkapselungen entweichen können und in das Zytoplasma, also das flüssige Innere der Zelle gelangen können .
Für medizinische und biotechnologische Anwendungen sind modifizierte Kohlenstoff-Nanoröhrchen von großem Interesse, da sie dank der veränderten Oberflächeneigenschaften normalerweise nicht überwindbare biologischen Barrieren jetzt durchdringen können. Im Vergleich zu nicht-modifizierten CNTs liegen die modifizierte Kohlenstoff-Nanoröhrchen in einer wässrigen Umgebung als einzelne Röhrchen vor und verklumpen nicht . Aufgrund ihrer Form und Größe könnten diese CNTs jetzt einen bislang noch nicht bekannten alternativen Eintrittsweg in die Zellen benutzen, der Vesikel-unabhängig ist. Neueren Studien haben belegt dass in der Lunge spezielle Surfactant Bestandteile (Proteine und Lipide) eine solche „biologische Funktionalisierung" von mehrwandigen Kohlenstoff-Nanoröhrchen bewirken. Die Zytotoxizität der mehrwandigen CNTs wird davon aber nicht beeinflusst .
Auf welchem Weg die Kohlenstoff-Nanoröhrchen die Zellen wieder verlassen oder ob sie in den Zellen akkumuliert werden, ist bis heute nicht geklärt.
Obwohl sie lediglich aus einem Kohlenstoffgerüst bestehen, gibt es bei den Kohlenstoff-Nanoröhrchen (CNTs) eine Vielzahl verschiedener Strukturen: einwandige und mehrwandige Röhren, Längen und Oberflächenbeschichtung. Diese vielen Variationsmöglichkeiten erschweren den direkten Vergleich des Umweltverhaltens. Sie liegen zudem oft nicht als einzelne Röhrchen, sondern als zusammengelagerte Bündel vor. Darum können nur schwer allgemeingültige Aussagen über das Umweltverhalten dieser großen Vielfalt an CNTs getroffen werden.
![Schematischer Überblick über die verschiedenen Struktur-Arten von Kohlenstoff-Nanoröhrchen: einwandig (SWCNT), mehrwandig (MWCNT) und auch mögliche Oberflächen-Modifikationen. © Angepasst mit Erlaubnis von Jackson, P et al. (2013). Bioaccumulation and ecotoxicity of carbon nanotubes. Chem Cent J, 7(1): 154. Open Access article [CC-BY-2.0 (http://creativecommons.org/licenses/by/2.0)]. Schematischer Überblick über die verschiedenen Struktur-Arten von Kohlenstoff-Nanoröhrchen: einwandig (SWCNT), mehrwandig (MWCNT) und auch mögliche Oberflächen-Modifikationen.](/wp-content/uploads/2020/10/CNT-Jackson-2013-DE.png)
Schematischer Überblick über die verschiedenen Struktur-Arten von Kohlenstoff-Nanoröhrchen: einwandig (SWCNT), mehrwandig (MWCNT) und auch mögliche Oberflächen-Modifikationen. © Angepasst mit Erlaubnis von Jackson, P et al. (2013). Bioaccumulation and ecotoxicity of carbon nanotubes. Chem Cent J, 7(1): 154. Open Access article [CC-BY-2.0 (http://creativecommons.org/licenses/by/2.0)] .Das Umweltverhalten der Kohlenstoff-Nanoröhrchen hängt stark von der Form und den Eigenschaften der Röhrchen ab. Sie können z.B. wasserlöslich oder wasserunlöslich sein, was ihr Verhalten in Gewässern entscheidend beeinflusst.
Unbeschichtete Kohlenstoff-Nanoröhrchen lösen sich kaum in Wasser und setzten sich daher schnell ab (sedimentieren). Ein verbesserte Wasserlöslichkeit und somit auch längere Verweildauer in Gewässern kann man durch Veränderung der CNT-Oberfläche erreichen, z.B. durch verschiedene Beschichtungen . Gelöste organische Substanzen (z.B. Zersetzungsprodukte abgestorbener Organismen) können in Oberflächengewässern mehrwandige Kohlenstoff-Nanoröhrchen stabilisieren, so dass diese nicht zum Grund des Gewässers absinken . Einen gegenteiligen Effekt bewirken Kalzium-Ionen. Sie führen zu einer Zusammenballung der Kohlenstoff-Nanoröhrchen zu größeren Bündeln, wodurch das Absinken beschleunigt wird .
Auch in Böden beeinflusst die Oberflächenbeschaffenheit der CNTs entscheidend den Verbleib. Einwandige Kohlenstoff-Nanoröhrchen weisen beispielsweise eine geringe Beweglichkeit auf, wenn ihre Wasserlöslichkeit durch eine bestimmte Beschichtung verbessert wurde. Die CNTs setzen sich dann aufgrund ihrer Faser-Form schnell ab und können sich bei einer möglichen Freisetzung im Boden kaum ausbreiten .
Kohlenstoff-Nanoröhrchen können ebenso wie andere bekannte Kohlenstoff-Materialien, beispielsweise Aktivkohle, sehr effektiv andere Stoffe binden und dadurch als Filter eingesetzt werden. Aufgrund dieser Eigenschaft können Kohlenstoff-Nanoröhrchen zahlreiche Umweltschadstoffe binden und anreichern . Einfluss auf die Schadstoffbindung haben zum einen der Schadstoff selbst , die verfügbare freie Oberfläche der Kohlenstoff-Nanoröhrchen sowie der Umfang der Oberflächenmodifizierung der CNTs . Ebenso kann die Bindung der Schadstoffe an die Kohlenstoff-Nanoröhrchen in Gegenwart von Kupfer-Ionen oder Surfactant beeinflusst werden . Kupfer-Ionen erhöhen die Schadstoffbindung, indem sie als „Brücke" die CNTs mit dem Schadstoff verbinden. Im Gegensatz dazu besetzen die Bestandteile des Surfactants die Oberfläche der Kohlenstoff-Nanoröhrchen, so dass kaum noch Platz für Schadstoffe bleibt. Im Vergleich zu Industrieruß werden die zu erreichenden Umwelt-Konzentrationen der CNTs als sehr gering eingeschätzt, weshalb auch nur eine geringe Schadstoffbindung durch CNTs zu erwarten ist .
Es gibt erste Hinweise darauf, dass Kohlenstoff-Nanoröhrchen durch bestimmte Pflanzen-Enzyme abgebaut werden können . Reine CNTs sind vor diesen Enzymen geschützt, während Kohlenstoff-Nanoröhrchen mit bestimmten Oberflächenmodifikationen (Carboxyl-Gruppen) gut abgebaut werden können.
Zusammengefasst ist das Verhalten von Kohlenstoff-Nanoröhrchen in der Umwelt stark abhängig von ihren Eigenschaften, wie Länge und Oberflächenbeschaffenheit. Außerdem treten die CNTs in der Umwelt mit zahlreichen anderen Stoffen in Wechselwirkung. Diese unterschiedlichen Verhaltensweisen wirken sich nachweislich auch auf die Art bzw. den Grad einer toxischen Wirkung gegenüber Umweltorganismen aus.
 >
>